Ландштайнер, Янский и Мосс (Landsteiner, Jansky, Moss) установили существование четырех кровяных групп среди нормальных людей. Эти четыре кровяные группы характеризуются, по мнению авторов, наличием в эритроцитах агглютиногенов А и В, а в сыворотке крови соответственных агглютининов А и В. Так как в одной и той же крови не могут находиться одноименный агглютинин и агглютиноген, то возможны четыре комбинации состава крови, согласно которым все человечество по крови делится на четыре группы. Несмотря на то, что биохимическая сущность, обусловливающая различие этих четырех видов крови, еще не установлена, однако практическое значение определения кровяной группы чрезвычайно велико, главным образом при переливании крови, когда необходимо знать, не обладает ли переливаемая кровь гемолитическими свойствами. Ввиду того что сыворотка, гемолизирующая эритроциты in vivo, обладает агглютинизирующими эритроциты свойствами in vitro, этими последними свойствами и пользуются при определении кровяных групп. В качестве реактива пользуются обычно двумя сыворотками — II и III, которые продаются в специальной упаковке. Контрольный гемотест выпущен в Вене; с ним сравниваются сыворотки, приготовленные в различных институтах.
Принадлежность к той или иной группе обусловливается генетическими особенностями — присутствием в эритроцитах гена А, В или АВ, или же отсутствием его. Шредер считает, что агглютиногены представляют собой липоиды, а агглютинины — евглобулины. Кристаллическая решетка соответственного гена обусловливает постоянное образование определенных агглютиногенов в строме эритроцитов. Количественно они вариируют в очень больших пределах как индивидуально, так и от различных внешних факторов, влияющих на организм человека; так, например, агглютинабильность эритроцитов повышается под влиянием физической работы, во время приступов малярии, при брюшном тифе и т. п. Растворение эритроцитов, высокая температура уничтожают агглютиногены, тогда как в засохшей крови они сохраняются. У зародыша человека накопление агглютиногена в эритроцитах идет медленно, так что принадлежность эмбриона к определенной группе можно установить, только начиная с шестого месяца. Интересно отметить, что в сыворотке плодов нет собственных агглютиногенов, а сыворотка новорожденного не агглютинирует крови матери (если она даже другой группы). Образование собственных агглютиногенов идет постепенно и заканчивается ко второму году жизни.

Схематически четыре группы крови по Янскому можно представить следующим образом (рис. 1).
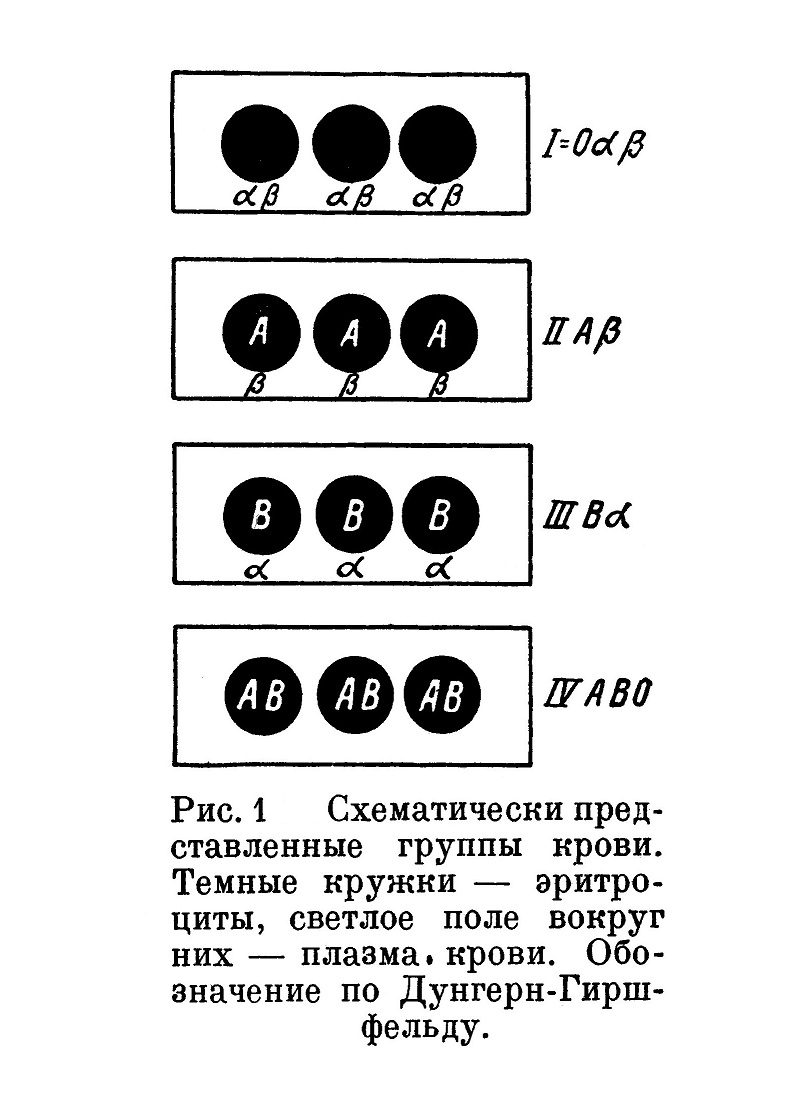
В настоящее время обозначением Моссе не пользуются. В бывшем СССР приняты обозначения Янского и Дунгерн-Гиршфельда.
Основные правила при переливании:
1. Кровь I группы можно переливать больному любой группы. Больному с кровью I группы можно переливать кровь только I группы.
2. Кровь IV группы можно переливать больному только IV группы. Больному с кровью IV группы может быть перелита кровь любой группы.
3. Кровь II группы можно переливать больному с кровью IV и II группы.
4. Больному с кровью III группы может быть перелита кровь III или I группы.
Приведенные основные правила, которыми нужно руководствоваться при переливании крови, становятся понятными, если мы будем исходить из того положения, что решающими являются свойства эритроцитов донора: эритроциты I группы не содержат агглютиногенов, поэтому какова бы ни была сыворотка реципиента, она не может их агглютинировать, resp. растворить. Что касается значения свойств сыворотки донора (которая, конечно, переливается вместе с эритроцитами), то здесь выступает значение высоты титра сыворотки. Для того чтобы сыворотка была активной в смысле агглютинации (resp. растворения) эритроцитов, нужно, чтобы она сохраняла эти свойства также при различных разведениях. Однако даже сыворотки с высоким титром не выдерживают таких разведений, какие получаются при переливании крови, — сыворотка крови донора разводится большим количеством сыворотки реципиента.
Сыворотка донора обычно инактивируется высоким разведением кровью реципиента и поэтому свойства сыворотки донора по отношению к эритроцитам реципиента не учитываются. Однако при резко выраженных анемиях, особенно после обильной кровопотери, количество крови реципиента может быть настолько малым, что не дает достаточного снижения титра сыворотки донора. В этих случаях можно получить гемолиз эритроцитов реципиента сывороткой донора.
Фуругата полагает, что наследуются не только гены А и В, но и свойства сывороток крови А и В в виде серии аллеломорфов (пар) из трех различных генов, могущих замещать друг друга в одном и том же месте одной из хромосом. В том гене, который генетиками связывается с агглютинацией, имеются одновременно радикалы молекул соответствующего группе агглютинина и агглютиногена — значит радикалы евглобулина и лецитиноподобного липоида. Генетический анализ различных групп семей показал, что наследование групп крови происходит по законам Менделя.
Кроме свойственных всем группам колебаний способности эритроцитов связывать агглютинин и агглютинироваться, Ландштайнер доказал наличие в гене А особых подгрупп А1 и А2, причем ген А1 является доминантным по отношению к гену А2 (рецессивному).
Открытый в 1940 г. Ландштайнером и Винером (Wiener) Rh-фактор определяется посредством сыворотки крови кролика, которому предварительно вводилась кровь обезьяны (Macaccus Rhesus); около 80% людей содержат в крови Rh-фактор.
При определении групп необходимо учитывать следующие моменты.
1. При температуре в 10° и ниже наступает так называемая холодная агглютинация — сыворотки агглютинируют эритроциты всех групп. В редких случаях холодная агглютинация наступает и при более высокой температуре воздуха, когда сыворотка начинает агглютинировать собственные эритроциты,— аутоагглютинация. В этих случаях не удается даже сделать подсчета эритроцитов в камере, так как агглютинация наступает уже в меланжере. От холодной агглютинации по существу отличается аутоагглютинация, наступающая в редких случаях анемии, по-видимому, вследствие патологического распада эритроцитов. Наличие в крови человека агглютинина холода не опасно потому, что амплитуда его действия никогда не превышает 25°, поэтому исключается возможность его действия при температуре тела. При определении группы крови агглютинины холода имеют значение, так как могут давать повод к диагностическим ошибкам. Поэтому сыворотки освобождаются от агглютинина холода тем, что свертывание крови производится при 0°, при этом агглютинины связываются с эритроцитами и не попадают в сыворотку.
2. Ложная агглютинация, т. е. зависящая от образования монетных столбиков, исчезает при прибавлении физиологического раствора.
Феномен Томсена заключается в наблюдении, что в некоторых случаях кровь при стоянии как бы изменяет свою группу; так, эритроциты группы О начинают агглютинироваться любой сывороткой. Этот феномен объясняется каталитическим процессом, обусловленным продуктами жизнедеятельности бактерий. Феномен Томсена имеет практическое значение, так как при переливании такой крови наступает гемолиз.
Техника. Обычно реакция производится на предметном стекле, на которое сначала наносится по капле сыворотки группы II и III, а затем к каждой капле прибавляется немного крови так, чтобы получилась розовая окраска. Употребляется или свежая кровь, или же, лучше, отцентрифугированные эритроциты крови, к которой был прибавлен лимонно-кислый натрий, или же кровь разводится 1% лимоннокислым натрием в десять раз в пипетке для счета белых кровяных телец. Сыворотка смешивается с кровью чистой стеклянной палочкой, и затем наблюдают 1 — 5 минут, слегка поворачивая стекло, чтобы мешать оседанию эритроцитов. Положительная реакция характеризуется выпадением эритроцитов в виде хлопьев. Шиф и Рубашкин считают, что определение на предметных стеклах нередко дает ошибки (псевдоагглютинация), и предлагают пользоваться серологической техникой определения в небольших пробирках; таким же образом производится проба с кровью получателя и донора на их взаимноагглютинационные свойства (сыворотка получателя + эритроциты донора). Последнюю пробу необходимо производить перед началом переливания крови.
Однако в некоторых случаях, несмотря на тщательное определение групп при переливании крови, все же получается гемолиз. Целый ряд авторов считает необходимым производить биологическую пробу (даже без предварительного установления групп).
Биологическая проба состоит в том, что в вену получателя (больного) вводится 10 см3 крови донора; если в продолжение нескольких минут не обнаруживается неблагоприятной реакции (беспокойство больного, рвота, ускоренный пульс и пр.), то приступают к переливанию необходимого количества крови. Абсолютной гарантии биологическая проба также не дает, так как известны случаи так называемого позднего гемолиза.
Большой опыт в переливании крови показал, что наиболее подходящей является кровь донора той же группы, так что кровью I группы пользуются не так широко. Несмотря на это, все же остаются случаи, когда даже самый тщательный подбор крови не предотвращает от неприятных осложнений — озноб, рвота, крапивница, астматический приступ; в крови — лейкопения. Нужно думать, что это явления аллергического порядка.
Выделенные в последнее время свойства крови М и N не имеют пока практического значения.
В основе стимулирующего действия переливания крови, по мнению Богомольца, лежит коллоидоклазия, т. е. физический феномен, выражающийся во взаимном осаждении белков плазмы донора и реципиента, что связано с явлением преципитации и флокуляции. Преципитации подвергаются, по мнению Богомольца, также состарившиеся белки протоплазмы клеток, которые после осаждения подвергаются ферментативному распаду. Таким образом, коллоидоклазия белков крови донора и белковых веществ клеточных элементов реципиента как бы служит стимулом сложной биологической реакции самоочищения клетки. В отличие от протеинотерапии, при которой в процесс коллоидоклазии вовлекаются и полноценные элементы крови, при трансфузии коллоидоклазичёский шок распространяется только на неполноценные элементы крови, на не-полноценные белковые мицеллы. Клинические проявления коллоидоклазии белков реципиента и донора зависят, по мнению Богомольца, от количества введенных белков и их способности флокулировать с белками реципиента. Можно наблюдать ряд градаций от самых легких реакций до смертельного коллоидоклазического шока, иногда сопровождающегося гемолизом, но могущего протекать и без всяких следов последнего. При патологогистологическом исследовании органов погибших от трансфузионного шока могут быть обнаружены (наряду с явлениями, сопровождающими любой интраваскулярный гемолиз) гемоглобинурическая почка (см. отравление мышьяковистым водородом), эритрофагия и сидероз ретикуло-эндотелия (главным образом селезенки и печени), а также явления, обычно встречающиеся при анафилактическом шоке, в первую очередь некрозы в печени. Таким образом, если и наступает микрофлокуляция, согласно коллоидоклазической теории Богомольца (причем, нужно думать, флокулируют также молекулы гемоглобина при выхождении его из эритроцитов), то они не являются субстратом, вызывающим непосредственно патологию в органах и тканях по типу закупорки капилляров. Декомпозиция плазмы крови является резким раздражителем для сосудистой, в первую очередь капиллярной, системы печени и почек; это является причиной тормозных процессов в клубочках почек —- вплоть до анурии, тогда как выпадение кровяного пигмента в мочевых канальцах является следствием, а не причиной наступившей анурии. Некрозы в печени развиваются путем ишемии, частью вследствие быстрого прекращения кровотока в сокращенных капиллярах, частью вследствие более медленной ишемизации с явлениями лейкоцитарных стазов и последующего некроза отдельных участков печеночной ткани.
 Занятие 1-е. Вакцины и анатоксины. Вопросы для обсуждения. 1. Искусственный иммунитет, активный и пассивный. 2. Препараты для создания искусственного активного иммунитета: вакцины и анатоксины. 3. Виды вакцин: живые, убитые и химические. 4. Способы приготовления вакцин. 5. Анатоксины нативные и очищенные, их получение и титрован... Читать далее... |
|