Микрофлора лекарственного сырья и готовых лекарственных форм. Обсемененность микробами растений, в том числе и лекарственных, может быть очень высокой и зависит от условий их произрастания, от характера растения, высоты стебля и других причин. Микрофлора растений, а следовательно, растительного лекарственного сырья чрезвычайно разнообразна. На поверхности растений обнаруживаются представители микрофлоры почвы, среди которых основное место занимают сапрофитные спорообразующие бактерии, актиномицеты и грибы.
 Особенно сильно заселяются микробами срезанные и сорванные растения. Среди микроорганизмов, встречающихся на растениях и в растительном лекарственном сырье, могут встречаться фитопатогенные виды, т. е. виды, вызывающие заболевания растений. Особенно сильно заселяются микробами срезанные и сорванные растения. Среди микроорганизмов, встречающихся на растениях и в растительном лекарственном сырье, могут встречаться фитопатогенные виды, т. е. виды, вызывающие заболевания растений.
Некоторые виды микроорганизмов, находящихся в растительном лекарственном сырье, обладают сильной ферментативной активностью. Они могут при соответствующих условиях разрушать фармакологически активные вещества, тем самым снижая ценность лекарства.
Консервирование лекарственного сырья и условия его хранения оказывают существенное влияние на его обсемененность. При хранении в условиях повышенной влажности микроорганизмы не только более длительно сохраняют жизнеспособность, но могут размножаться и изменять физические и химические свойства лекарственного сырья. Порчу лекарственного сырья обнаруживают по изменению цвета, появлению очагов размножения плесени и пр.
Лекарственные препараты, изготовляемые на фармацевтических заводах и в аптеках, в различной степени обсеменены различными микроорганизмами. Количество микробов в лекарствах сильно варьирует в зависимости от ряда причин — от обсеменности сырья, формы препарата, от особенностей изготовления, от санитарного состояния аптечного учреждения. Известную роль в загрязнении лекарственных препаратов могут играть дистиллированная вода, посуда, пробки, руки аптечных работников, а также воздух аптечных лабораторий. Поэтому большое значение придается периодическому микробиологическому контролю в аптеках, который проводится санитарно-эпидемиологическими станциями.
Стерильные инъекционные растворы могут обладать пирогенными свойствами, т. е. вызывать повышение температуры тела. Это обусловлено наличием в них убитых бактерий или продуктов их распада. В связи с этим дистиллированная вода для приготовления инъекционных растворов не должна содержать в 1 мл более 10—15 бактерий (приказ Министерства здравоохранения СССР № 573, приложение 1—3, от 30 ноября 1962 г.).
Среди готовых лекарственных форм наиболее обсемененными являются препараты растительного происхождения — настои и отвары. При хранении этих лекарств, особенно в теплом месте, количество микробов в них возрастает до высоких цифр и появляются признаки порчи: муть, пленка, изменение цвета, необычный запах.
Бактерии обнаруживаются в настойках, растворах солей, а из порошкообразных препаратов особенно обсемененными является тальк, крахмал, сахар, зубной порошок.
При изготовлении лекарств следует учитывать источники и пути их загрязнения и создавать условия, исключающие возможность микробного загрязнения. Для предупреждения микробного загрязнения некоторые лекарства (например, глазные капли) следует изготовлять в асептических условиях, пользоваться стерильной посудой и соблюдать стерильность при их укупорке.
Для определения микробной загрязненности лекарственных средств разработана методика, утвержденная приказом Министерства здравоохранения СССР и Министерства медицинской промышленности (приказ № 944/486/207 от 10 октября 1974 г.). Согласно этой методике, лекарственные не инъекционные средства должны подвергаться бактериологическому исследованию на количество сапрофитных бактерий, дрожжевых и плесневых грибов и наличие бактерий следующих родов и видов: Proteus, Escherichia, Salmonella, Shigella, Pseudomonas aeruginosa, Staphylococcus aureus.
Образец для бактериологического исследования (10 г или 10 мл) должен быть взят не менее чем из 10 упаковок. Его разводят фосфатным буферным раствором (pH 7,0) до объема 50 мл (разведение 1:5). 25 мл полученного раствора или суспензии разводят до 50 мл тем же буферным раствором (разведение 1:10). 1 мл этого разведения разводят еще в десять раз (разведение 1 : 100).
Для количественного определения сапрофитных бактерий на чашки Петри с мясо-пептонным агаром засевают по 0,5 мл разведений 1 : 10 и 1:100. Колонии подсчитывают через 48 ч пребывания посевов в термостате при 37°С.
Для определения количества дрожжевых и плесневых грибов производят посев на чашки Петри со средой Са- буро по 0,5 мл разведения 1:5 и 1:10.
Раздельный подсчет колоний дрожжевых и плесневых грибов производят через 5 сут пребывания посевов при 20—22°С.
Для обнаружения бактерий рода Proteus 0,5 мл разведения 1 : 10 вносят в конденсационную воду свежескошенного агара (посев по Шукевичу). При наличии ползучего роста через 24—48 ч выделяют чистую культуру и проводят ее идентификацию.
Методы выделения и идентификации бактерий кишечно-тифозного семейства (Escherichia, Salmonella, Shigella) описаны в соответствующих статьях данного раздела сайта.
Для выделения Pseudomonas aeruginosa и Staphylococcus aureus 1 мл разведения 1:10 вносят в накопительную среду и после инкубирования в течение 24 ч при 37°С делают высев на соответствующие дифференциальные среды и изучают свойства стафилококков.
Питательные среды, используемые при бактериологическом исследовании лекарств. Среда Сабуро: к 1 л дистиллированной воды добавляют 10 г пептона, 40 г глюкозы или мальтозы, 1,5% агара. Среду стерилизуют при 110°С в течение 30 мин. Накопительная среда для выделения Staphylococcus aureus и Pseudomonas aeruginosa. В 1 л дистиллированной воды растворяют 5 г дрожжевого экстракта, 20 г казеинового гидролизата, 5 г хлорида натрия, 10 г пептона, 2 г глюкозы, 2,5 г двухзамещенного фосфата натрия. Среду стерилизуют при 120°С в течение 15 мин.
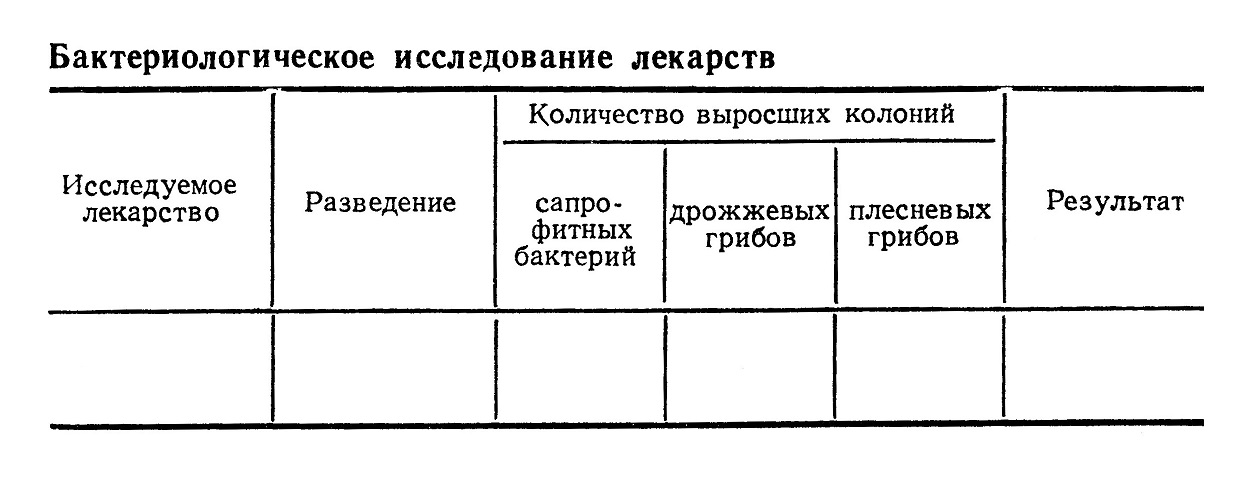
На практических занятиях студенты проводят количественное определение сапрофитных бактерий, дрожжевых и плесневых грибов в различных образцах лекарств. Чашки с посевами помещают с термостат, затем раздельно подсчитывают количество выросших колоний сапрофитных бактерий, дрожжевых грибов и плесневых грибов. Результаты исследования оформляют в виде табл.
 Занятие 1-е. Вакцины и анатоксины. Вопросы для обсуждения. 1. Искусственный иммунитет, активный и пассивный. 2. Препараты для создания искусственного активного иммунитета: вакцины и анатоксины. 3. Виды вакцин: живые, убитые и химические. 4. Способы приготовления вакцин. 5. Анатоксины нативные и очищенные, их получение и титрован... Читать далее... |
|  Особенно сильно заселяются микробами срезанные и сорванные растения. Среди микроорганизмов, встречающихся на растениях и в растительном лекарственном сырье, могут встречаться фитопатогенные виды, т. е. виды, вызывающие заболевания растений.
Особенно сильно заселяются микробами срезанные и сорванные растения. Среди микроорганизмов, встречающихся на растениях и в растительном лекарственном сырье, могут встречаться фитопатогенные виды, т. е. виды, вызывающие заболевания растений.