Ретикуло-эндотелиальная система состоит из петель ретикулярной ткани (основы всех кроветворных органов), из активного эндотелия, выстилающего венозные синусы, а также из активных перителиальных клеток и блуждающих клеток в покое рыхлой соединительной ткани. Как синцитий ретикулярных петель, так и эндотелиальные, resp. гистиоцитарные, клетки функционируют согласно двум источникам раздражения, которые они получают: под влиянием раздражения, идущего через оплетающий и пронизывающий их нервный аппарат, ретикуло-эндотелиальная ткань диференцируется в миэлогенные, эритробластические и лимфоидные элементы, тогда как под влиянием поступающих с кровью веществ в ретикуло-эндотелиальной ткани активируется выработка внутриклеточных энзимов, ферментов, наступает внутриклеточное изменение концентрации водородных ионов [Питталуга (Pittaluga)]. Этим же путем поступают в ретикуло-эндотелиалъную ткань различные витамины - А, D и С, которые частью фиксируются и являются важным звеном ее жизнедеятельности, частью вновь поступают в кровяное русло, поддерживая, таким образом, витаминный баланс других тканей и органов. В последнее время особенно выдвигается роль ретикуло-эндотелия в липоидном балансе организма не только в смысле отложения липоидов, но и в выработке специальных липоидов.
Здоровый организм на различных стадиях жизни характеризуется более или менее определенной формой обмена веществ; последний в свою очередь определяет состояние ретикуло-эндотелиальной системы.
В постэмбриональном периоде и во все последующие периоды жизни ретикуло-эндотелиальная система сохраняет, по существу, все свои функции периода эмбрионального развития организма.
Положение, что ретикуло-эндотелиальная система сохраняет в постнатальном состоянии кроветворную функцию и что никакой другой мезенхимой с кроветворными функциями взрослый организм не обладает, подтверждают многочисленные работы последних лет, касающиеся патологии ретикуло-эндотелиальной системы. Поведение органов и тканей при патологических процессах, повторяя в гипертрофированном виде физиологические процессы, нередко проливают свет на течение трудно уловимого в своей последовательности развития отдельных форменных элементов крови и на их взаимоотношения в норме. Так, патология нам показывает, что синцитий ретикулярной ткани под влиянием особого формативного раздражителя (типа карциногенного вещества) дает своеобразные гиперплазии-ретотелиозы или опухоли - ретотелиомы, resp. ретотельсаркомы. Лозовский описывает ретикуло-эндотелиальный саркоматоз как системное заболевание ретикуло-эндотелия. Наряду с гиперплазией и опухольным ростом ретотелия с несомненностью выступает его диференциация в кровяные элементы с клинической и патологоанатомической картиной лейкемии [Алъстром, Луберс (Ahlstrom, Lubbers) и др.].
Наблюдая за поведением ретикуло-эндотелия при различных заболеваниях, мы убедились, что синцитий ретикулярной ткани, образующий остов кроветворных органов, а в патологических случаях развивающийся из гистиоцитов соединительной ткани в различных органах и тканях, особенно в коже и в подкожной жировой клетчатке, обладает чрезвычайно выраженной потенцией к кроветворению всех видов клеток, тогда как эндотелий венозных синусов селезенки такой потенцией не обладает.
Таким образом, коротко формулируя, мы должны сказать, что:
1. Ретикуло-эндотелий сохраняет и эмбрионально, и постнатально кроветворные свойства активной мезенхимы.
2. Образовавшиеся эмбрионально-родоначальные клетки различных типов форменных элементов крови: миэлобласты, лимфобласты, эритробласты, монобласты, быстро исчерпываются как кроветворный фонд; постоянное наличие их в кроветворных органах объясняется тем, что количество их постоянно пополняется неизменно кроветворно функционирующей ретикуло-эндотелиальной тканью.
3. Направленность функции ретикуло-эндотелия обусловливается специфической сенсибилизацией эндотелия капилляров соответствующего участка ретикуло-эндотелия; этим и объясняется, например, сегментарное расположение очагов эритробластической и миэлогенной ткани (см. костный мозг).
4. Мобилизация кровяных элементов, переход их из кроветворных органов в кровь, обусловливается и регулируется фактором обратной проницаемости эндотелиального барьера капилляров (кроветворная ткань — капилляр).
5. Тогда как при физиологических условиях кроветворно активным является главным образом ретикуло-эндотелий кроветворных органов, при патологических условиях сенсибилизируется ретикуло-эндотелий и других органов, в первую очередь печени и пульпы селезенки.
Следовательно, никакой миэлогейной, resp. лимфоидной, метаплазии органов и тканей в смысле пробуждения к жизни каких-то эмбриональных зачатков мезенхимальной ткани нет, да и никто их в действительности не видел.
Благодаря более строгому разграничению функций отдельных органов заложенная в них ретикуло-эндотелиальная ткань или развивает имеющиеся в ней потенции, сенсибилизируется, или же, наоборот, становится менее чувствительной к функциональным раздражениям. Так, функцию кроветворения при здоровом состоянии организма выполняет главным образом ретикулярная и периваскулярная тканъ, находящаяся в костном мозгу и фолликулах лимфатических желез и селезенки. При повышении физиологического раздражителя усиливается пролиферация кроветворных элементов в пределах этих органов. В патологических случаях активируется ретикуло-эндотелий и других органов, в первую очередь печени и селезенки; наконец, в зависимости от характера раздражителя появляются очаги кроветворения в самых различных тканях и органах. Инфекционный процесс нередко ведет к развитию лимфоидных и миэлогенных разрастаний — воспалительная реакция. Рёссле (Rossle) очень удачно назвал воспаление «очагами парэнтерального пищеварения». Вокруг инородных тел ретикуло-эндотелий образует гигантские клетки; лангансовские гигантские клетки туберкулезных бугорков образуются, как это особенно наглядно наблюдается в культуре тканей, частью из ретикуло-эндотелия, частью из мононуклеаров.
Большое значение для функции ретикуло-эндотелия имеет количество имеющихся в клетках витаминов. Так, например, при наличии большого количества витамина А в купферовских клетках (что выявляется флюоресценцмикроскопией) значительно увеличивается способность этих клеток откладывать трипановую синьку. Богатство витамином D увеличивает способность ретикуло-эндотелия вырабатывать эритроциты [Каллас (Каіlath)].
Активность ретикуло-эндотелия в процессе межуточного обмена по локализации распределяется следующим образом: наиболее активным является эндотелий лимфатических синусов лимфатических желез и венозных синусов селезенки и костного мозга — «Uferzellen», прибрежные клетки по Зигмунду (Siegmund), а также капилляры печени, коры надпочечников и придатка мозга. В этих клетках перевариваются отжившие белые и красные кровяные тельца, что особенно резко выступает в патологических случаях с усиленным распадом кровяных телец, когда указанные ретикуло-эндотелиальные клетки резко увеличены в объеме и выполнены фагоцитированными лейкоцитами и эритроцитами. Переваривание идет, по всей вероятности, ферментативным путем; продукты переваривания частью сохраняются более или менее продолжительное время в протоплазме клетки, частью (нужно думать вместе с ферментами) Выделяются в кровь, resp. в лимфу. Таким образом, появляются в крови как продукт секреции ретикуло-эндотелиальных клеток, например, гемолизины. Участие ретикуло-эндотелия в обмене веществ, в нейтрализации токсинов и в выработке иммунных тел происходит путем так называемого ультрамикроскопического фагоцитоза. Гортега (Hortega) выделил при помощи специальной окраски ткани центральной нервной системы особые клетки — микроглии, обладающие резко выраженной .фагоцитарной способностью. Гортега считает, что микроглия происходит из мезенхимы (в противоположность эктодермальной глии) и является ретикуло-эндотелиальным аппаратом центральной нервной системы.
По Гортега, микроглия появляется в мозгу животных только в последнем периоде эмбриональной жизни или даже в первые дни после рождения путем миграции гистиоцитарных клеток мягкой мозговой оболочки в ткань мозга. Гортега не исключает возможности происхождения микроглиоцитов и из моноцитов крови.
Образование так называемых антител признается различными авторами одной из функций ретикуло-эндотелия.
Можно допустить, что выделяемые ретикуло-эндотелием ферменты изменяют коллоидальное состояние плазмы крови и тем самым изменяют ее иммунобиологические свойства. В выработке местного тканевого иммунитета также участвует ретикуло-эндотелий соответственных тканей в виде заложенных повсюду в соединительной ткани гистиоцитов, блуждающих клеток в покое. Чрезвычайно трудно установить, насколько велико участие кровяных элементов в выработке иммунных свойств организма; несомненно, однако, что они живо реагируют при патологических процессах в организме, способны фагоцитировать, переваривать и т. п. Гемопоэтический ретикуло-эндотелий кроветворных органов хотя и в несколько меньшей степени, но тоже непосредственно участвует в нормальном межуточном обмене. В патологических случаях он резко активируется, понижая при этом свою кроветворную деятельность; так, например, при некоторых заболеваниях ретикулярные клетки лимфатических желез настолько гипертрофируются и загружаются липоидами, что ткань железы гистологически почти сплошь состоит из ретикулярных элементов, а лимфоидные клетки почти совершенно исчезают.
Эндотелий, выстилающий различные полости: плевральную, брюшную, сердечную, спинномозговой канал, и эндотелий, выстилающий сосудистые сплетения мозга, принимает живое участие как в нормальном, так и в патологическом обмене. Сенсибилизированный эндотелий серозных оболочек при повторном действии токсинов нередко становится местом локализации воспалительного процесса. Наименее активным и не поддающимся сенсибилизации является эндотелий периферических сосудов; однако как клиника, так и эксперимент дают яркие примеры активирования ретикуло-эндотелиальных элементов интимы сосудов [Дитрих (Dietrich)]. Активированный ретикулярный эндотелий выделяет вещества, которые могут послужить закладкой тромба.
Эндотелий сосудов, а также соединительнотканная основа внутренней оболочки сосудов (интимы) получают питательные вещества непосредственно из крови того сосуда, который выстилают, так как капилляры vasa vasorum не проникают в стенку сосуда дальше средней его оболочки (mediae), интима же лишена кровеносных капилляров (так же как и эндокард сердечных клапанов). Таким образом, интима сосудов, особенно венозных, благодаря особенностям, питания а priori не может быть везде одинаковой; она должна видоизменяться соответственно органу, в котором она заложена и продуктами жизнедеятельности которого она питается. Патология органов не может не отражаться на их сосудах. В резких случаях морфологически это выражается гиперплазией элементов интимы, отложением различных веществ (пигментов, липоидов и др.), а также явлениями дегенерации. Тромбоз сосуда является одним из следствий реактивного изменения эндотелия (например, тромбоз воротной вены печени).
Остальная часть ретикуло-эндотелиальной системы заключает, в себе гистиоциты (блуждающие клетки в покое, полибласты, плазмоциты и другие синонимы этих клеток), находящиеся повсюду в соединительной ткани, а также гистиоциты, расположенные вокруг сосудов (адвентициальные, перителиальные клетки и ретикулярные клетки лимфоидной и миэлогенной ткани).
Участие ретикуло-эндотелия в развитии и росте злокачественных новообразований в настоящее время усиленно обсуждается, однако мнения авторов по этому вопросу пока разноречивы.
Богомолец предлагает активировать ретикуло-эндотелий при злокачественном новообразовании впрыскиванием малых (раздражающих) доз цитотоксической антиретикулярной сыворотки. Последняя получается введением животным экстракта селезенки человека. В этом же направлении ведутся также работы по терапии лейкемий. При изучении функции ретикуло-эндотелиальной системы пользуются так называемой «блокадой» ее, имеющей целью функциональное выключение ретикуло-эндотелия загрузкой его различными веществами (красками, липоидами, тушью, вакциной и т. п.). Опыты на животных показали, что вряд ли можно таким образом действительно функционально выключить ретикуло-эндотелиалъную систему, так как при этом расширяется ее сеть вследствие сенсибилизации других пассивных элементов, а быстро наступающая гиперплазия ткани в избытке возмещает загруженные элементы; кроме того, ретикуло-эндотелий постепенно освобождается от поглощенных веществ путем переваривания их или же путем их выделения. Янчо (Jancso) экспериментально выключает ретикуло-эндотелиальную систему введением электроколлоидального раствора меди — элективного яда ретикуло-эндотелия.
По исследованиям Карбалло (Carballo), такого рода блокада получается только у мышей. Наиболее выраженная блокада в настоящее время получена комбинацией торотраста и коллоидной меди.
Далее Янчо показал в опыте на животных, что введением гепарина можно прекратить фагоцитарную функцию ретикуло-эндотелия — ни. тушь, ни колларгол не откладываются в ретикуло-эндотелии, пока продолжается действие гепарина.
Функциональной пробой фагоцитарной способности ретикуло-эндотелия является отложение в нем конгорота.
По разнице окраски сыворотки крови, полученной через 4 минуты и через 1 час после введения в вену 10,01% раствора конгорота колориметром Дюбоска или Аутенрита, определяется «конгорот-индекс», который в норме у человека равен 11—80.
Конгорот в свежеприготовленном, стерилизованном и профильтрованном растворе (лучше фильтровать два раза) обычно не дает болезненных явлений; однако некоторой токсичностью конгорот несомненно обладает, и после внутривенного введения краски нельзя быть гарантированным от неприятных осложнений, как, например, озноб, высокая температура и тяжелое общее состояние.
У туберкулезных больных функциональное исследование ретикуло-эндотелиальной системы конгоротом не дает каких-либо определенных закономерностей. При септических инфекционных заболеваниях, а также при различных формах нарушений кровообращения, при заболеваниях печени, при удалении селезенки количество растворенной в плазме краски при конгоротовой пробе повышается [Адлер, Рейнман и Виленский (Adler, Reinmann, Wilensky)].
Фагоцитарная способность ретикуло-эндотелиальной системы и особенно ее способность накоплять (Speicherung) резко изменяются под влиянием различных гормонов. Так, например, инсулин усиливает накопление веществ в ретикуло-эндотелии, препараты щитовидной железы — снижают его. Гольдман (Goldmann) получил под влиянием интерренина очень сильное отложение холестерина, тогда как питуитрин не оказывает влияния на отложение холестерина, усиливая в то же время отложение железа. Спленэктомия и оварэктомия создают оптимальные условия для блокады ретикуло-эндотелиальной системы. Наоборот, при блокаде ретикуло-эндотелиальной системы коллоидами, чтобы получить судороги от инсулина, нужно принимать значительно большие дозы последнего. Самарас (Samaras) показал, что после подкожного введения адреналина кроликам они становятся чувствительнее к туши, при этом понижается отложение ее в ретикуло-эндотелиальной системе.
Онтиверес (Ontiveres) находит, что ретикуло-эндотелий продуцирует вещества, ускоряющие свертываемость крови.
Чрезвычайно важную роль играет фагоцитарная деятельность ретикуло-эндотелиальной системы также при отравлении химическими, не бактериального происхождения, токсическими веществами. Последние откладываются в ретикуло-эндотелиальных клетках в большинстве случаев, нужно думать, в нетоксическом состоянии. При гистологическом исследовании микрохимическими реакциями устанавливается присутствие в клетках того или другого элемента, например, серебра — после введения колларгола, электраргола, мышьяка — после введения различных мышьяковистых соединений и т. п. Химическое же соединение как таковое не определяется. Значительно расширяется в настоящее время возможность выявления различных веществ в тканях методом спектроскопии и рентгеноскопии. Химический анализ органов и тканей при различных отравлениях также дает отцет только относительно наличия основного вещества, входящего в состав токсического начала. Так, например, при различных свинцовых отравлениях, дающих совершенно различную клиническую картину отравления, химическое исследование устанавливает то или иное распределение свинца в органах и тканях. Распространено мнение, что там, где произошло отложение, например, свинца, там же произошло и действие того свинцового соединения, которое дало определенную картину отравления. Нужно думать, что эти два процесса могут протекать независимо друг от друга; так, например, отложение свинца, в слизистой оболочке десен (свинцовая кайма) или в костях вовсе не свидетельствует о поражении этих тканей свинцом; точно так же действие свинца на костный мозг в случаях свинцовой анемии не стоит ни в какой зависимости от степени отложения свинца в ретикуло-эндотелии костного мозга.
Из краткого обзора развития кроветворных органов и клеток крови мы видим, что кроветворная ткань занимает особое место среди других тканей. В то время как эпителиальная ткань, например, проделав цикл своего эмбриологического развития, поддерживает свой status quo тем, что гибнущие клетки замещаются путем деления соседних клеток, кроветворная ткань как. бы постоянно находится в периоде развития. Возьмем хотя бы костный мозг трубчатых костей: в спокойном состоянии он состоит из жировой ткани, но когда организм теряет, например, много крови или заболевает инфекционной болезнью, — вновь развивается функционирующий костный мозг не только с различными кровяными клетками, но и с характерным ретикулярным строением, с фагоцитами и. т. д. Из каких же элементов идет реконструкция органа. Несомненно, из единичных недиференцированных мезенхимальных клеток, заложенных в соединительнотканных прослойках жировой ткани. Эти мезенхимальные клетки под влиянием определенного раздражения диференцируются так же, как это имеет место во время эмбрионального развития. Только так можно объяснить и постоянно вновь появляющиеся лимфоидные образования в виде фолликулов.
Костный мозг. Благодаря своему анатомическому положению — внутри кости, — костный мозг должен сохранять постоянный объем, поэтому в нем при различных функциональных состояниях изменяются только взаимоотношения между отдельными его составными частями. Наиболее лабильной при этом является жировая ткань, которая гипертрофируется или атрофируется, в зависимости от состояния специфической паренхимы органа и связанной с ней кровеносной системы. В последние годы в костном мозгу выявлена неврогенная сеть, лимфатических же сосудов в ней до сих пор не обнаружено. Микроскопически при усиленной деятельности, например, в остром периоде заболевания, костный мозг и в трубчатых костях красный вследствие расширения кровеносных сосудов, часто с кровянистой инфильтрацией ткани. По мере разрастания миэлогенной ткани костный мозг становится серо-красным, желтовато- серым, в некоторых случаях гноевидным. При кахексии костный мозг становится студенистым, желеобразным вследствие дегенеративных изменений жировой ткани. Атрофический костный мозг нередко становится фиброзным вследствие разрастания фибриллярной соединительной ткани с последующим гиалинозом волокон. При нормальном темпе кроветворения в костном мозгу плоских костей трудно установить какие-либо структурные особенности в строении миэлогенной ткани — в срезе превалируют зрелые элементы нейтрофильного ряда, местами эозинофилы, реже базофилы; эритробласты — единичные и скоплениями.
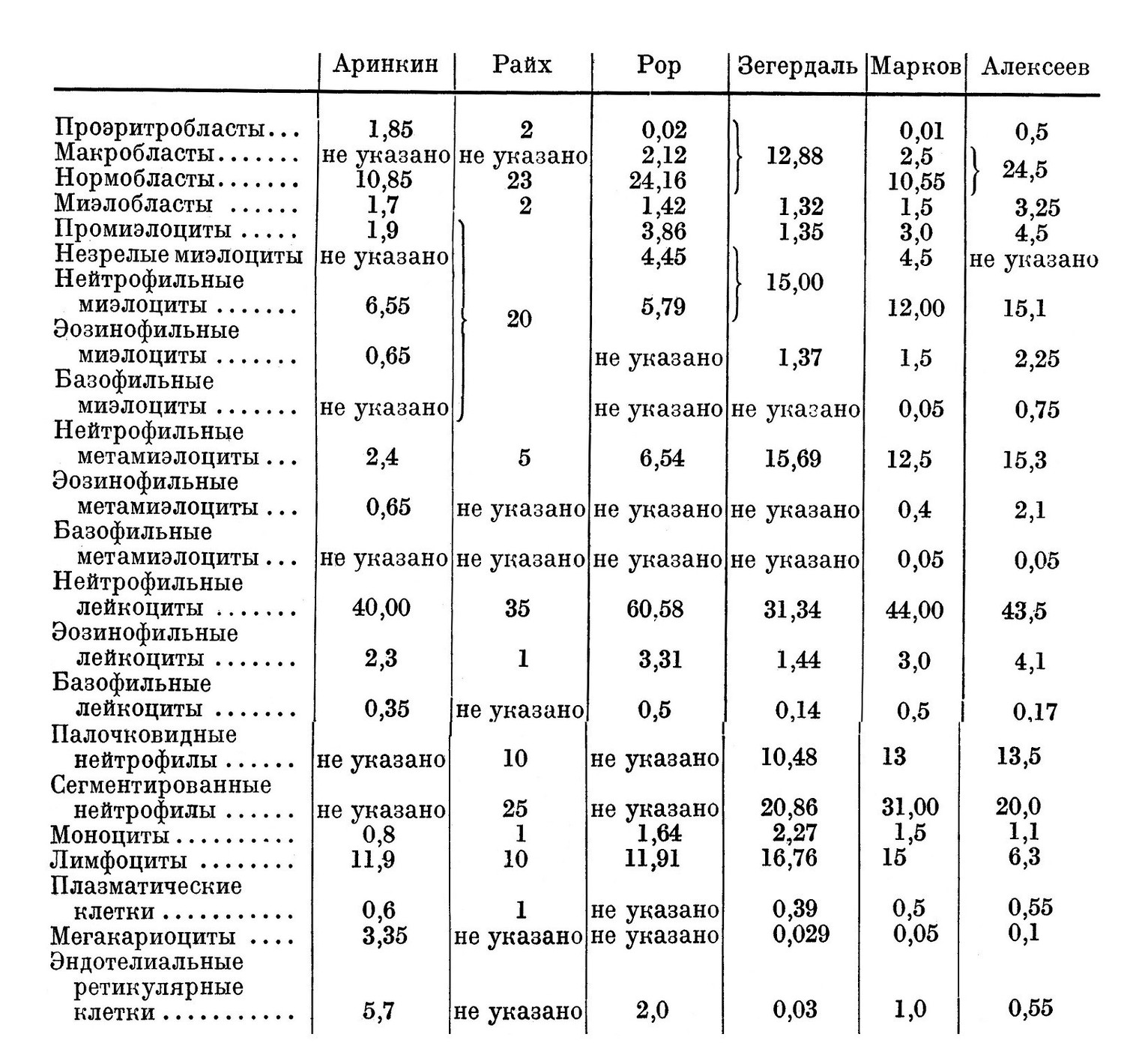
Приводим данные морфологического состава пунктата костного мозга, полученные различными авторами (средние цифры в процентах).
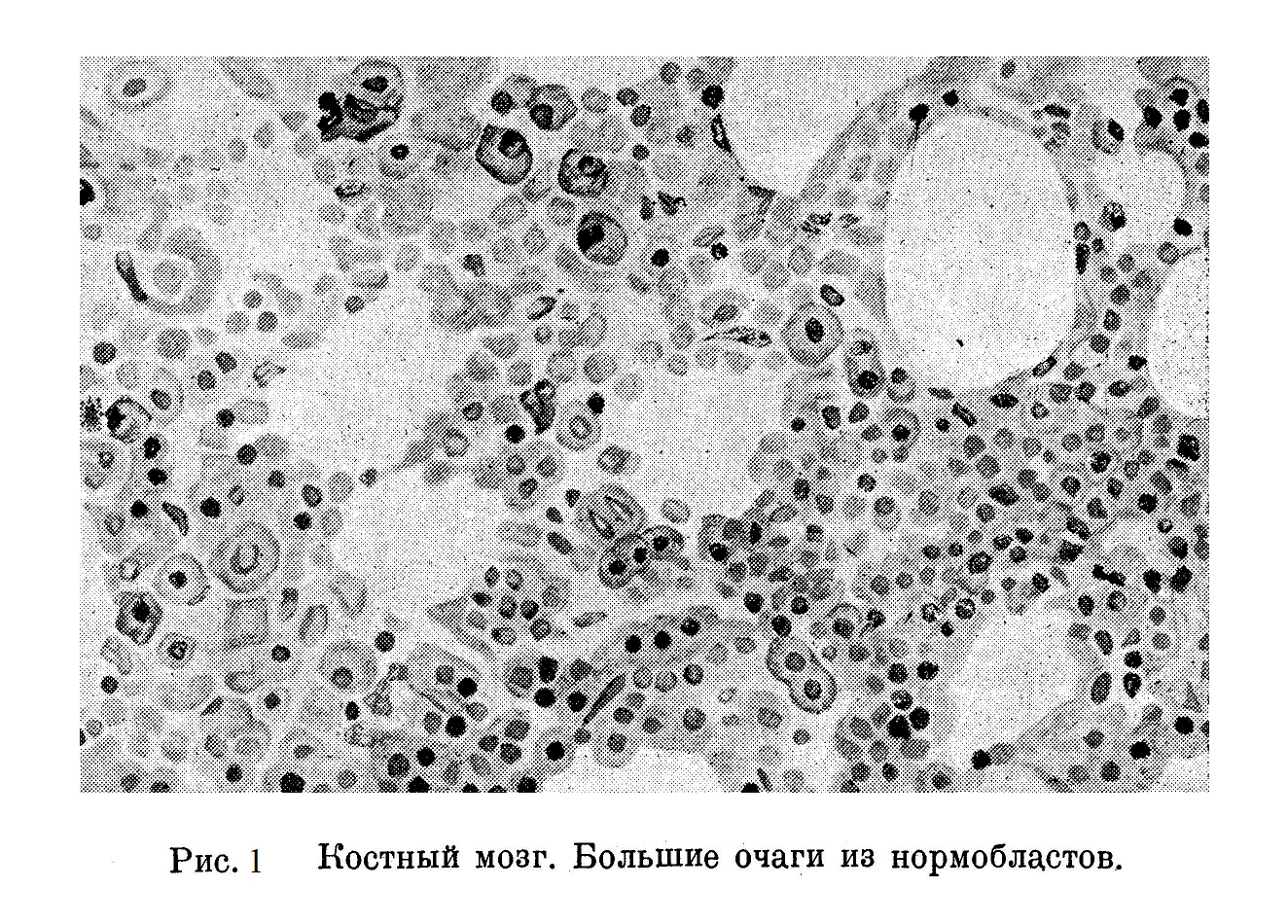
При усиленном образовании красных кровяных телец, не выходящем, однако, из пределов нормального типа кроветворения, выступает сегментарность эритропоэза в виде больших очагов эритробластов, довольно правильно чередующихся с лейкобластическими участками (рис. 1).
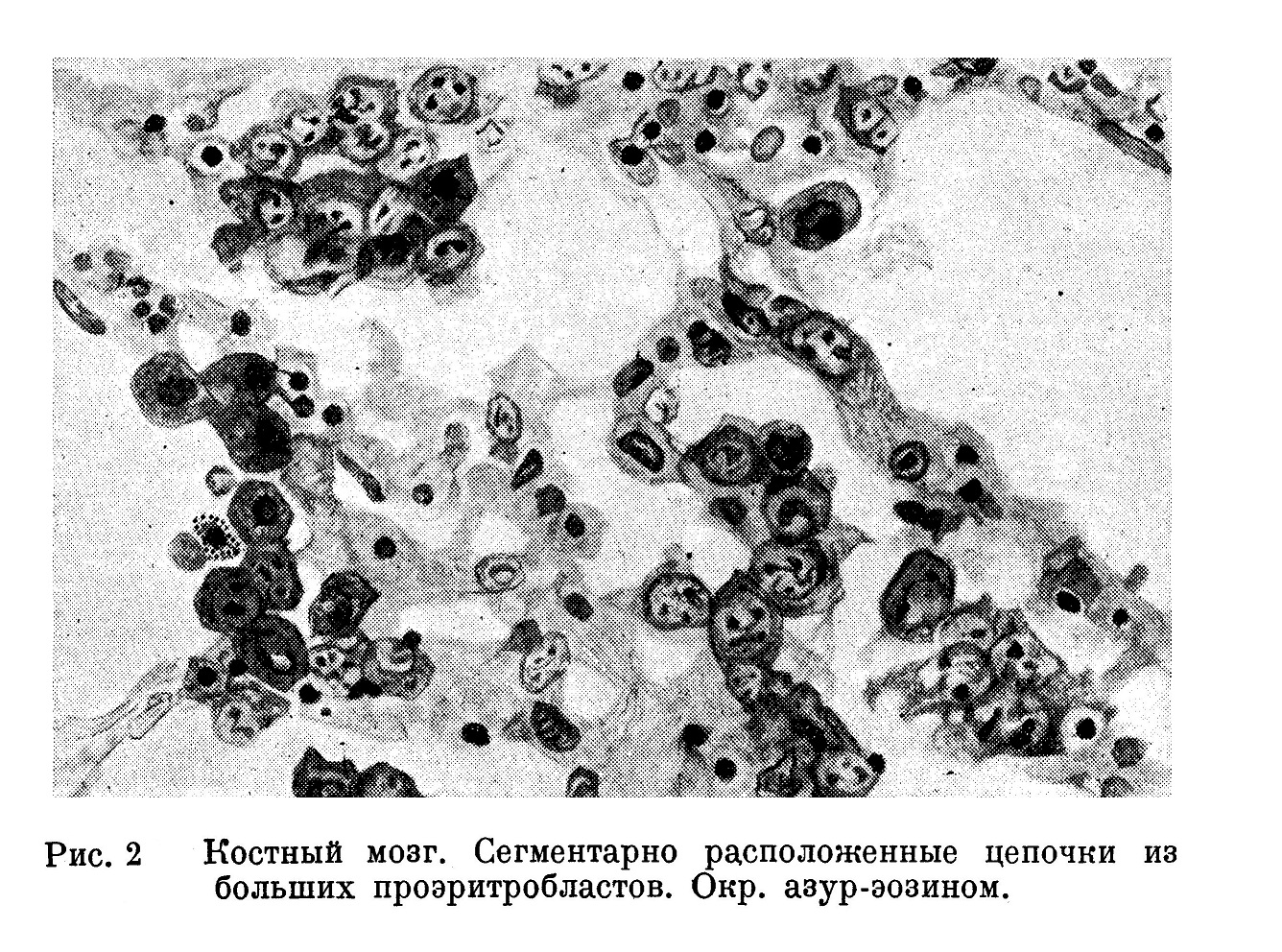
Значительно резче сегментарный характер кроветворения выступает при тяжелых анемиях с макро- и мегалоцитарного типа кроветворением, встречающимся как при пернициозной анемии, так и при других формах анемий (при лимфогранулематозе, лейкемиях, тромбопениях и др.), когда эритробласты выступают в виде характерных тяжей из больших клеток, богатых базофильной протоплазмой; на мазках протоплазма этих клеток местами с характерным сиреневым оттенком. Эти тяжи придают рисунку среза тигроидный вид (рис. 2).
Нахождение тяжей из отдельных больших эритробластов в пунктате костного мозга нередко ведет к неправильному диагнозу. Их принимают за мегалобласты. Сегментарность кроветворения с чередованием очагов эритробластических и лейкобластических дает ключ к пониманию диссоциированной функции этих двух систем: каждая система имеет свою иннервацию, регулирующую ее функцию.
Костный мозг, бедный клеточными элементами, может быть: 1) слабо функционирующим, вырабатывающим мало кровяных элементов, с незначительным поступлением их в кровяное русло и 2) костный мозг может функционировать даже усиленно, но если поступление клеток в кровяное русло настолько усиленно, что миэлогенная ткань не успевает вырабатывать запасных клеток, костный мозг становится бедным форменными элементами (рис. 3). Характерным для такого псевдоапластического мозга является большое количество плазматических клеток, происходящих из гистиоцитов.
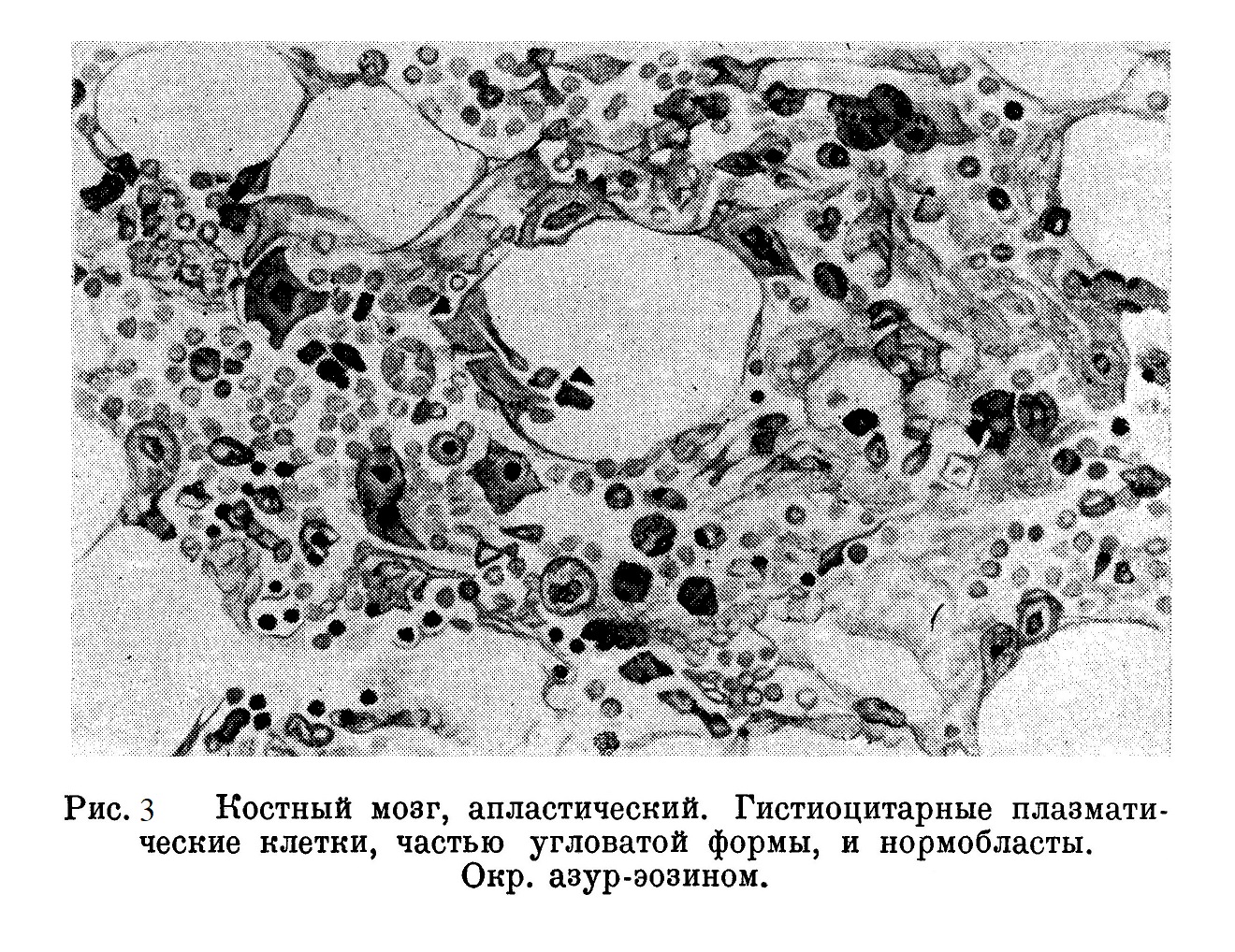
В настоящее время в клиниках и больницах стали нередко применять пункцию костного мозга как с диагностической целью, так и с научно-исследовательской. Чтобы правильно использовать данные, полученные путем пункции костного мозга, необходимо тщательно проработать морфологическую структуру костного мозга в норме и в патологии. Добывается костный мозг из грудины, у детей иногда пунктируют большеберцовую кость. Костный мозг грудины обычно является активным красным мозгом в продолжение всей жизни человека. Однако в грудине, как и в ребрах, нередко наблюдаются участки жировой ткани. Эту возможность получения из грудины жирового костного мозга при нормальном кроветворении остального активного костного мозга необходимо, конечно, учитывать. По мазку костного мозга подсчитывается процентное содержание форменных элементов и сравнивается с таблицей нормы, приводимой различными авторами. Если мы сравним данные нормы миэлограммы Аринкина для эритробластов (5,7 — 16,2%) с данными Райха и Рора (23 — 24,16%), то нужно признать, что широта колебаний очень велика. При исследовании костного мозга на трупном материале мы получаем чрезвычайно большие колебания процентного отношения клеток в мазках, взятых из различных участков. Наконец, в мазках костного мозга мы получаем главным образом свободно лежащие в тканях клетки, тогда как фиксированные клетки и ретикуло-эндотелий попадают только при большей или меньшей разрыхленности ткани. При этом в шприц могут попасть и кусочки костного мозга, которые всегда желательно исследовать гистологически на срезах.
Мы уже говорили, что основой костного мозга служит его reticulum, петли которого прикреплены частью к стенке кровеносных сосудов, частью к пластинкам эндоста. Между петлями находится незначительное количество соединительной ткани, главным образом вокруг кровеносных сосудов. Свою опорную функцию ретикулярная ткань выполняет благодаря тому, что звездчатые ретикулярные клетки образуют нежные фибриллы, которые, переплетаясь друг с другом, дают мелкопетлистую структуру. В зависимости от, функционального состояния, ретикулярная ткань дает различную гистологическую картину. Костный мозг изучается на тонких срезах, хорошо окрашенных азур-эозином. Показателем правильности окраски служит четкость структуры ядер, синяя окраска протоплазмы молодых клеток, четкая окраска нейтрофильной зернистости, а также зернистости мегакариоцитов в вишневокрасный цвет. На рис. 4 видны сочные петли reticulum, местами с выраженным синцитиальным строением; в синцитий диференцируются, а затем отделяются от него плазматические клетки.
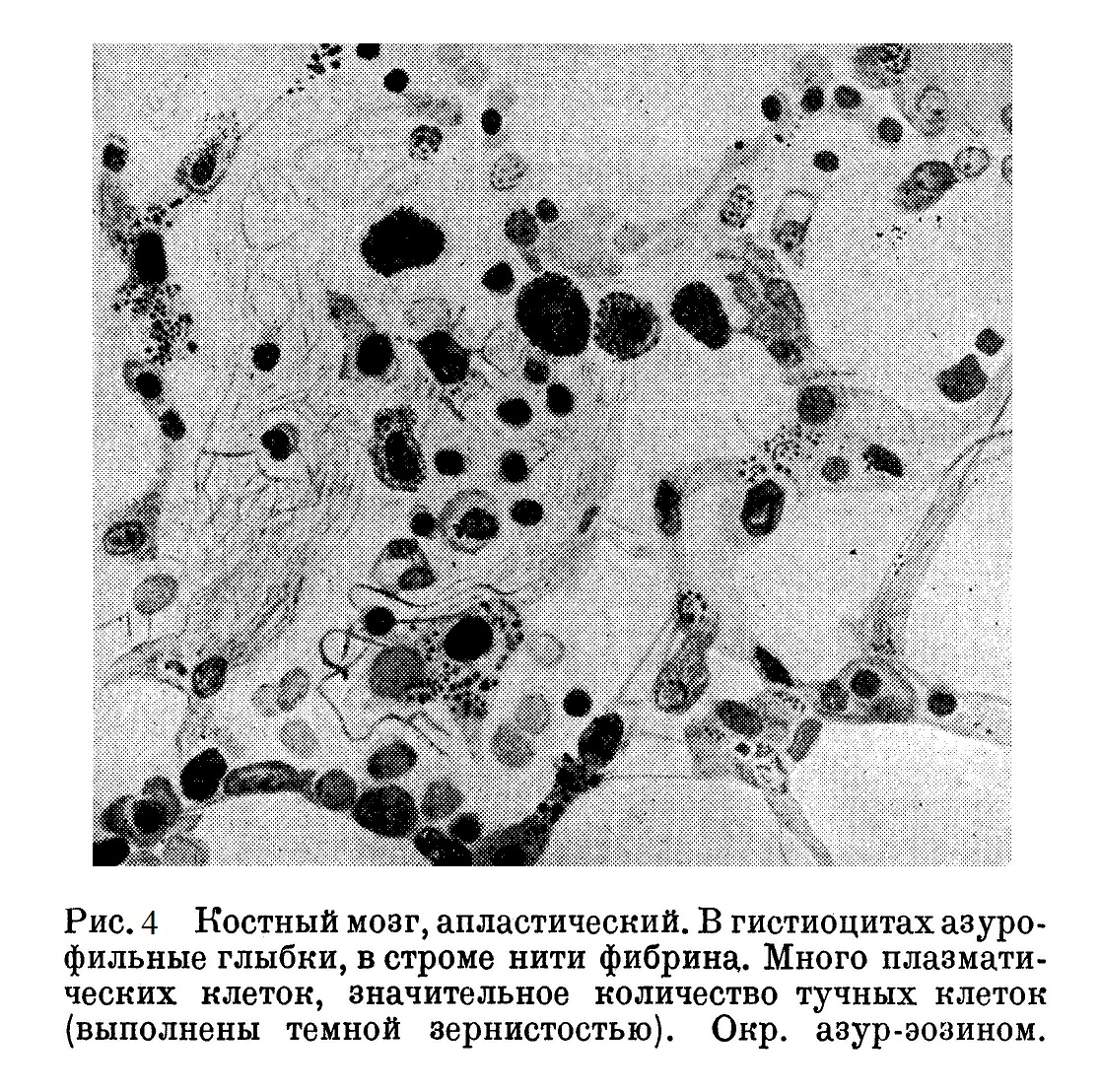
Здесь получается структура, аналогичная той, которую мы имеем в тканевой культуре ретикулярной ткани. Так же выглядит reticulum, когда резко заторможена его кроветворная функция — костный мозг крайне беден гранулоцитами. В протоплазме ретикулярного синцития часто обнаруживаются более или менее крупные глыбки, интенсивно окрашенные азуром в вишнево-красный цвет. Нужно думать, что эти глыбки являются продуктами межуточного обмена ретикуло-эндотелия. В случаях длительного торможения кроветворения может развиться так называемое фибриноидное перерождение ретикулярной ткани. На рис. 5 видно, как волокна, исходящие из ретикулярных клеток, принимают фибриноидный характер. Местами из ретикулярной клетки как бы выходит фибриноидная розетка. Возникает вопрос, не находится ли это «фибриноидное перерождение» в связи с функцией ретикуло-эндотелия образовывать фибриноген.
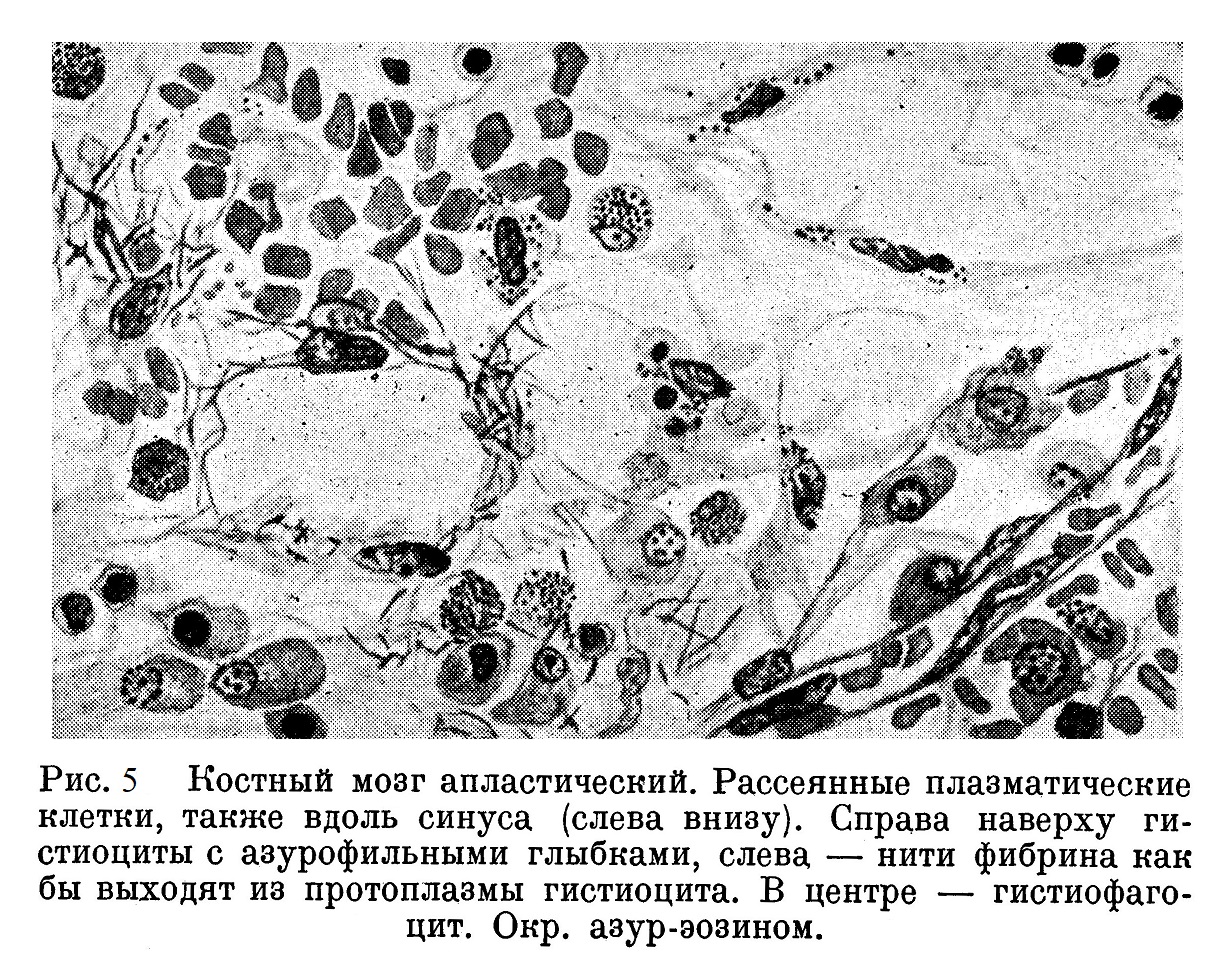
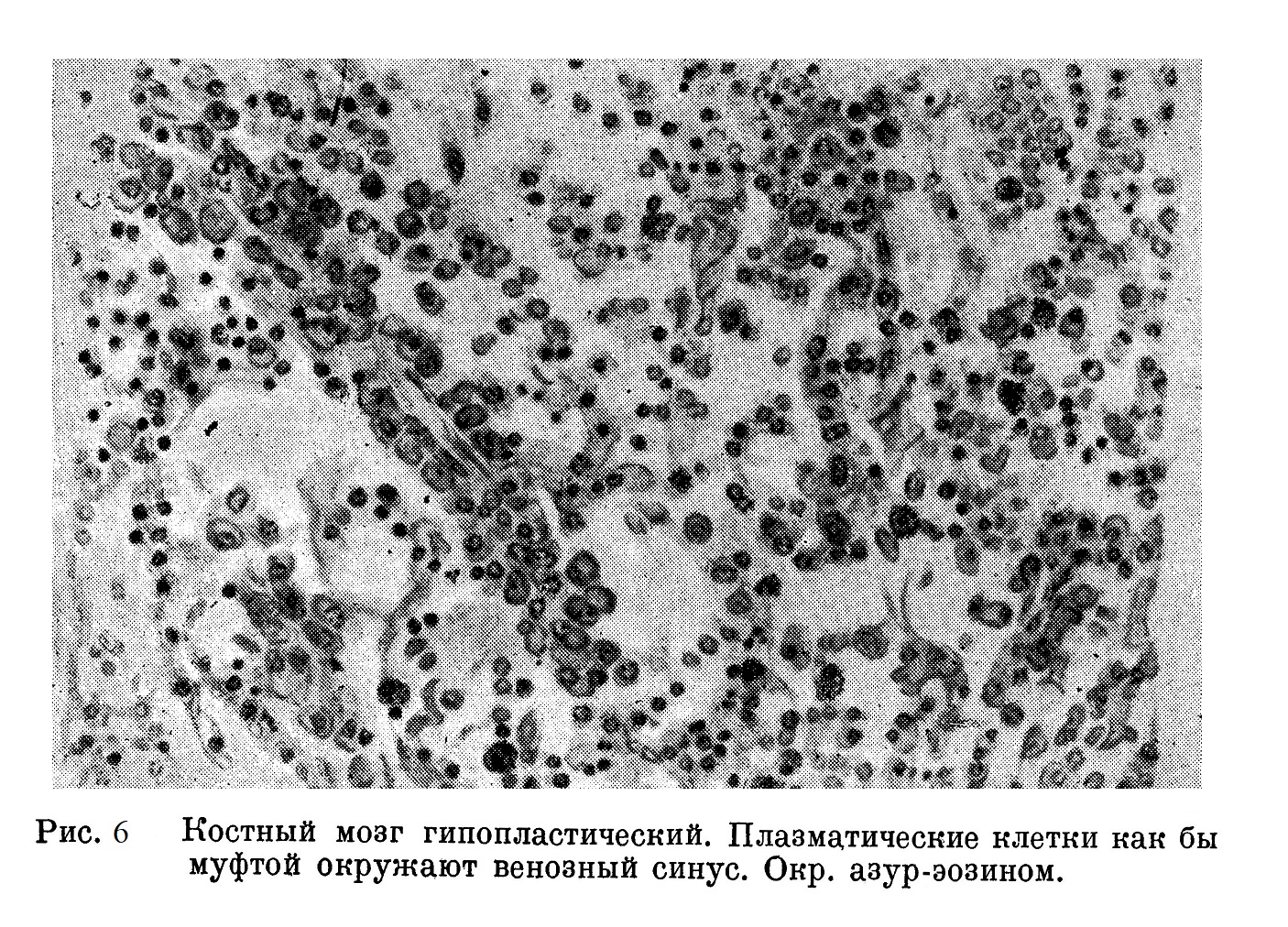
Нужно отметить, что при описанной выше морфологической картине заторможенного костного мозга постоянно наблюдается значительное количество лимфоидных клеток, диффузно рассеянных по всей ткани костного мозга. Лимфоидные клетки образуются наряду о плазматическими клетками (рис. 6) из ретикулярного синцития, имеют крайне невыразительное ядро, очень интенсивно окрашенное, и синюю протоплазму. Нужно думать, что большая часть этих клеток представляет собой мало диференцированные гистиоцитарные элементы, местами они, однако, группируются с хорошо выраженными эритрогониями, и, по всей вероятности, часть их принадлежит к этому виду клеток. Мы знаем, что под видом лимфоидной клетки могут скрываться всевозможного происхождения клетки. Так например, до 1910 г. все патологоанатомы признавали клетки «лимфосаркомы» надпочечников за лимфоциты, признавали до тех пор, пока Райт не доказал, что они являются симпатогониями (ганглиозные клетки). Поэтому, имея перед собой лимфоидного типа клетку, нужно быть крайне осторожным с диагнозом лимфоцита и только из совокупности особенностей различных однотипных клеток и всего препарата составлять суждение о природе данных клеток.
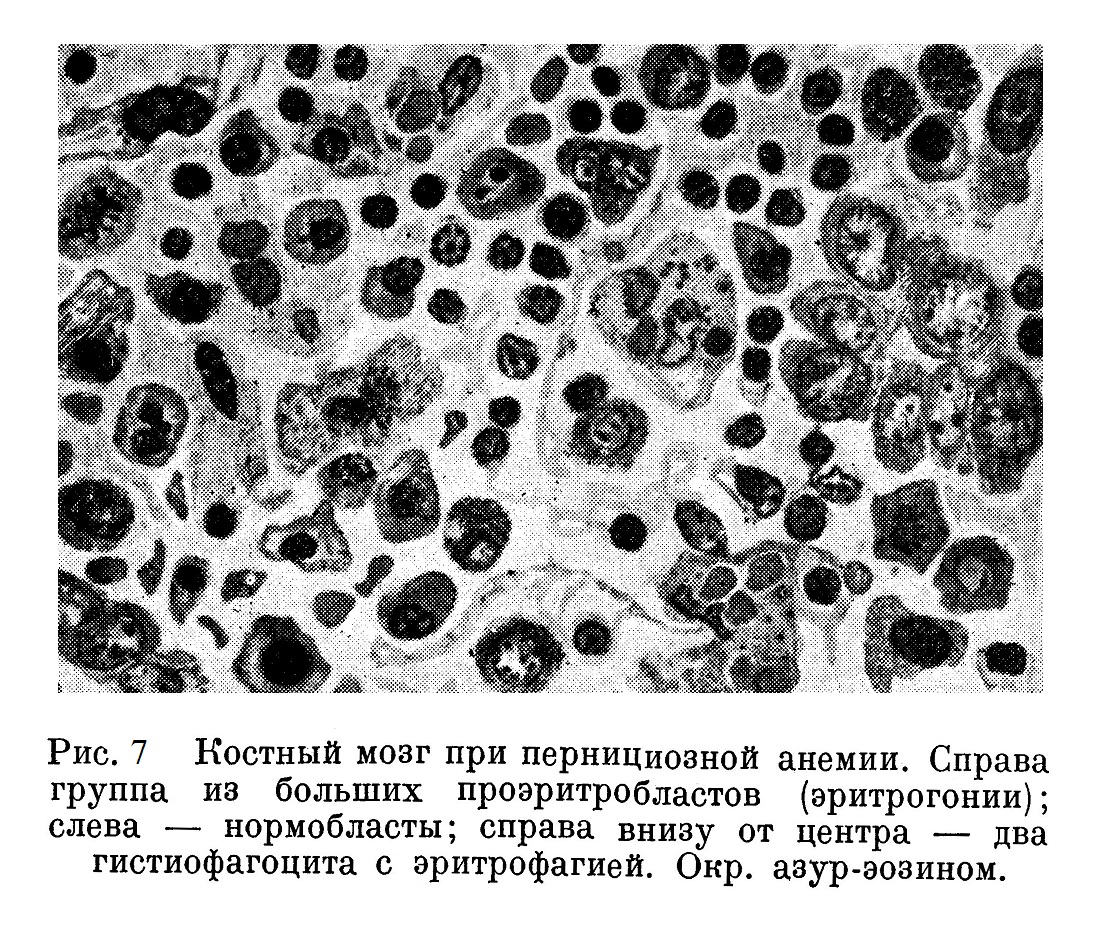
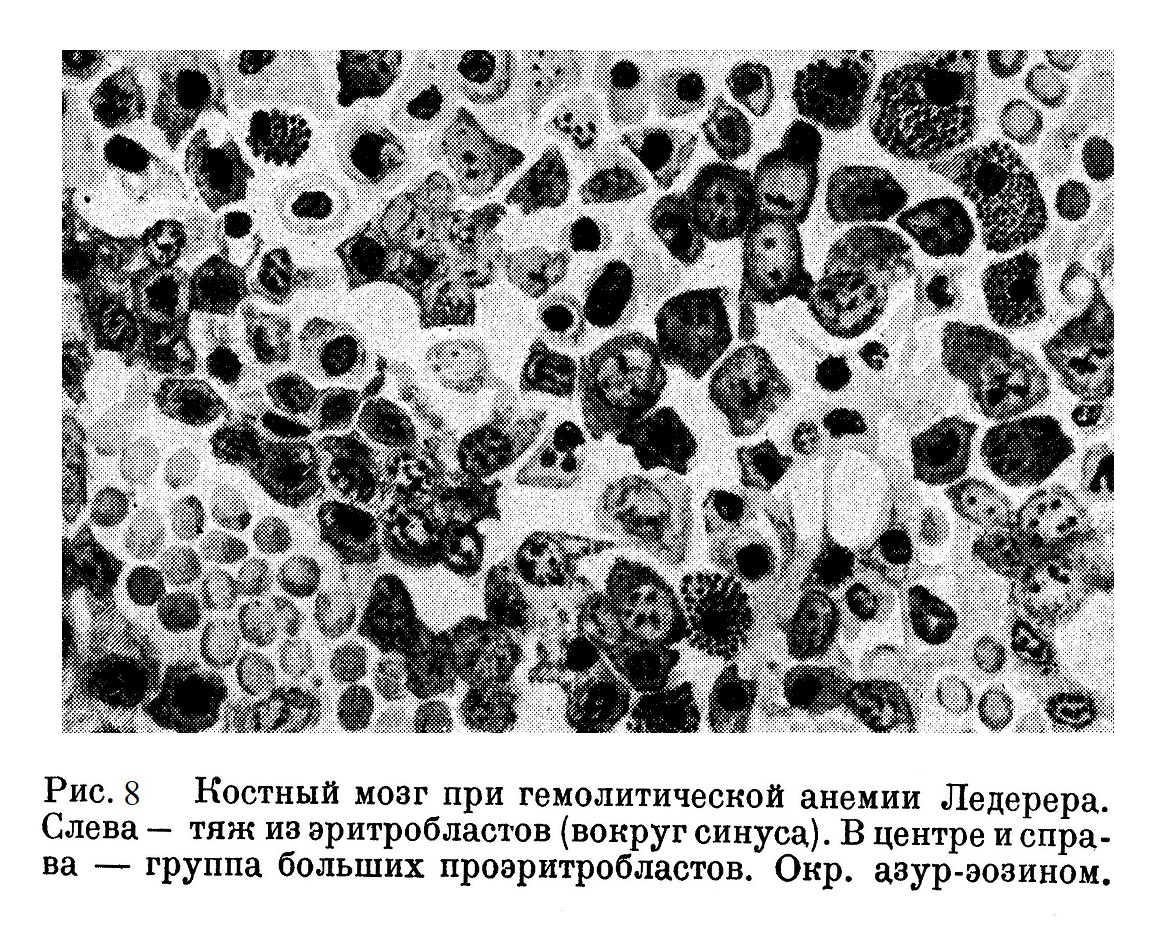
Что касается эритробластического кроветворения, то при нормальном темпе эритропоэза (около 900 биллионов эритроцитов в день) обнаруживаются небольшие скопления нормоэритр об ластов и рассеянные в ткани нормобласты; ядро эритробластов обычно круглое, богато базихроматином, часто располагающимся в виде колеса. При усиленной регенерации при анемии очаги эритробластов часто бросаются в глаза благодаря звездчатому рисунку их ядер — глыбчатый распад — кариорексис. Гелли (Helly) видит в такого рода распаде ядра выявление дегенерации, мешающей нормальному растворению ядра в протоплазме эритробласта. В циркулирующей крови при наличии в ней эритробластов нередко приходится наблюдать причудливой формы ядра эритробластов; они, однако, не носят характера гомогенных глыбок, которые мы обычно видим при кариорексисе отмирающего ядра. Вторым характерным признаком анемии является образование тяжей и гнезд из различной величины эритрогоний. На рис. 7 видны большие эритрогонии при пернициозной анемии; на рис. 8 изображен участок костного мозга, состоящий главным образом из средней величины эритрогоний, частью расположенных вокруг кровеносного сосуда, — случай тяжелой гемолитической анемии Ледерера. Отдельные гнезда из эритрогоний встречаются при самых различных анемиях, протекающих главным образом подостро (подострые лейкемии, лимфогранулематоз и др.). Морфологическая структура эритрогоний: большое ядро с характерным расположением базихроматйна на светлом фоне; ядро окружено ободком синей протоплазмы, местами амебоидной формы.
Эллерман (Ellermann) считает определяющим для вида клетки ее особую форму митоза, которую он измеряет величиной угла ахроматического веретена при делении. Согласно его данным, средний угол у мегалобластов равен 18°, у эритрогоний — 21°, у лимфобластов — 38—42°, у нейтрофильных миэлоцитов — 66—73°, у миэлобластов — 68°. В костном мозгу зародыша человека нам приходилось встречать гнезда из эритрогоний в небольшом количестве и не постоянно. Нормобласты с фрагментированными ядрами встречаются у зародышей иногда в большом количестве. Характерные различия морфологических форм эритропоэза при анемии мы объясняем не различием морфологического субстрата, из которого они развиваются, а изменением характера раздражения, которое получает кроветворный аппарат, — при заторможенной функции эритрогонии остаются на этой ранней ступени развития, тогда как при нормальном ходе развития эта стадия чрезвычайно быстро преходяща.
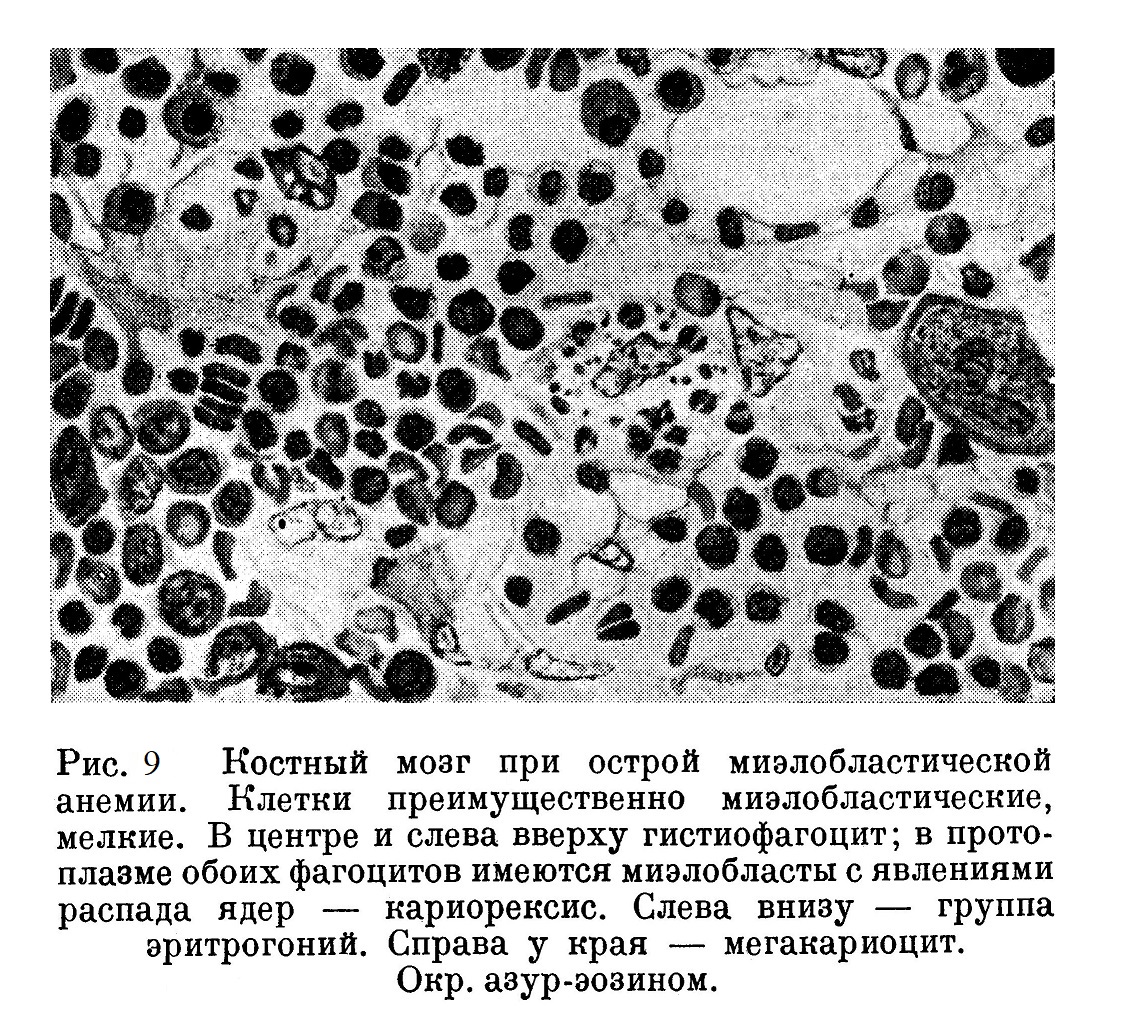
Говоря о характерных гистологических особенностях эритробластического кроветворения при различных формах анемии, необходимо подчеркнуть, что эти особенности выявляются лишь в отдельных частях костного мозга — характерные участки на большом количестве срезов нужно точно так же выискивать, как в мазках крови при пернициозной анемии приходится искать характерные мегалобласты или мегалоциты. Это относится также к особенностям лейкобластического кроветворения. При дисплазии гранулоцитарной системы, например, при остром миэлозе, наблюдается однотипно миэлобластический костный мозг (рис. 9); миэлобласты с характерным ядром и синей протоплазмой превалируют среди клеточных элементов; местами ядра распадаются, приобретают форму полулуния или кофейного боба и фагоцитируются крупными ретикулярными клетками, образующими петлистую основу костного мозга. Изредка обнаруживаются гнезда из эритрогоний, отдельные эритробласты, миэлоциты, лейкоциты, плазматические клетки, единичные мегакариоциты с пикнотическими ядрами небольших размеров, но с выраженной зернистостью протоплазмы. В некоторых случаях подострой миэлобластической лейкемии (хлорома), наряду с миэлобластическим костным мозгом, обнаруживаются очаги, состоящие почти сплошь из эозинофилов.
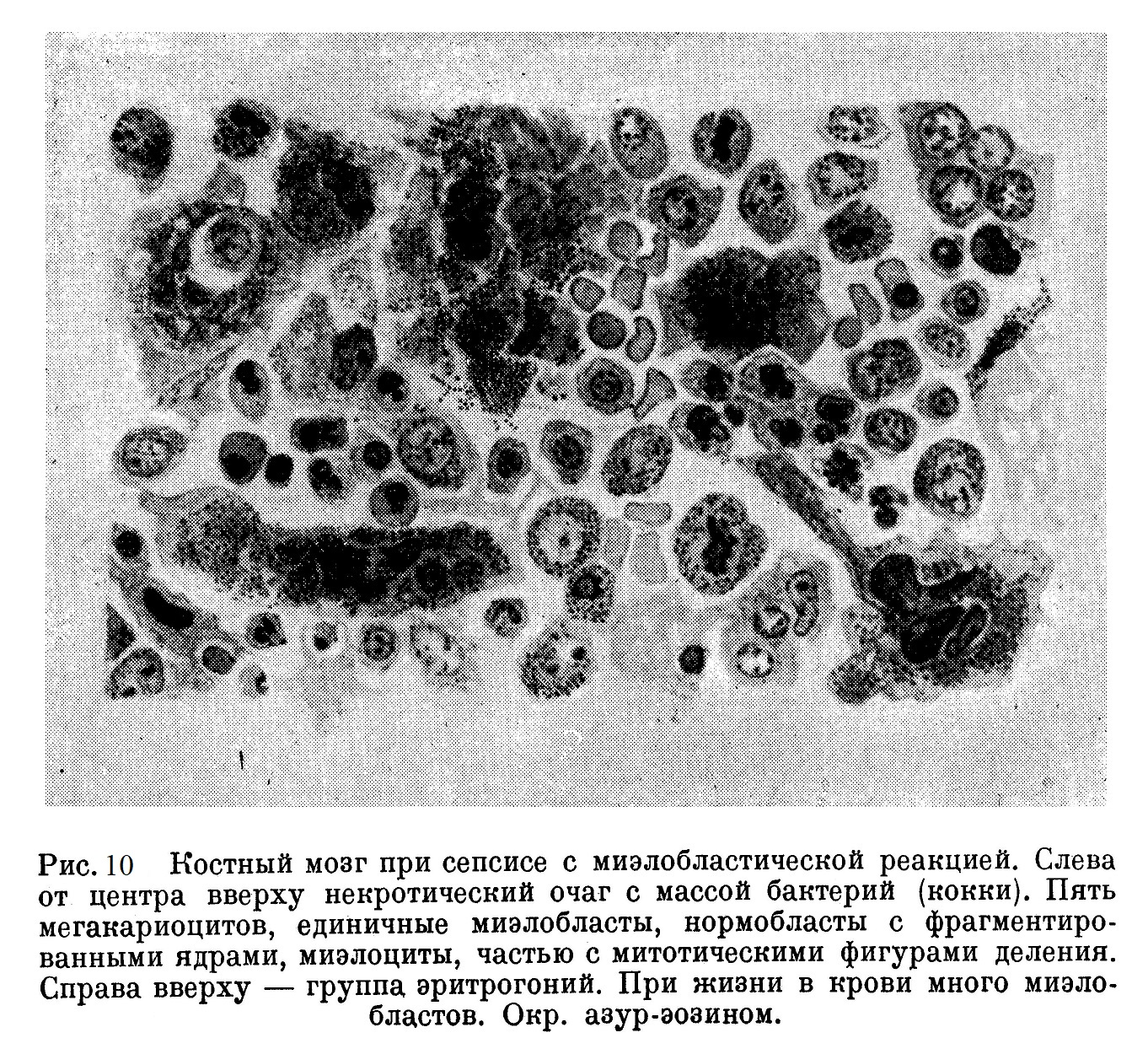
На рис. 10 изображен костный мозг в случае орального сепсиса, дававшего при жизни большое количество миэлобластов в крови и резкую тромбопению; костный мозг почти всюду богат миэлоцитами и мегакариоцитами. Исследуя костный мозг в случае лейкемии, протекавшем с очень высокими цифрами кровяных пластинок, частью с выраженной атипией, мы имели возможность выявить ряд Характерных особенностей мегакариоцитов, составлявших местами большинство клеток в поле зрения (при слабом увеличении) громадных размеров, с большим светлым ядром и зернистой протоплазмой, образующей большое количество псевдоподий; эти клетки местами оставляют впечатление как бы заживо распадающихся на пластинки клеточных образований; в крови при жизни больной наблюдались соответственные крупные бесформенные кровяные пластинки.
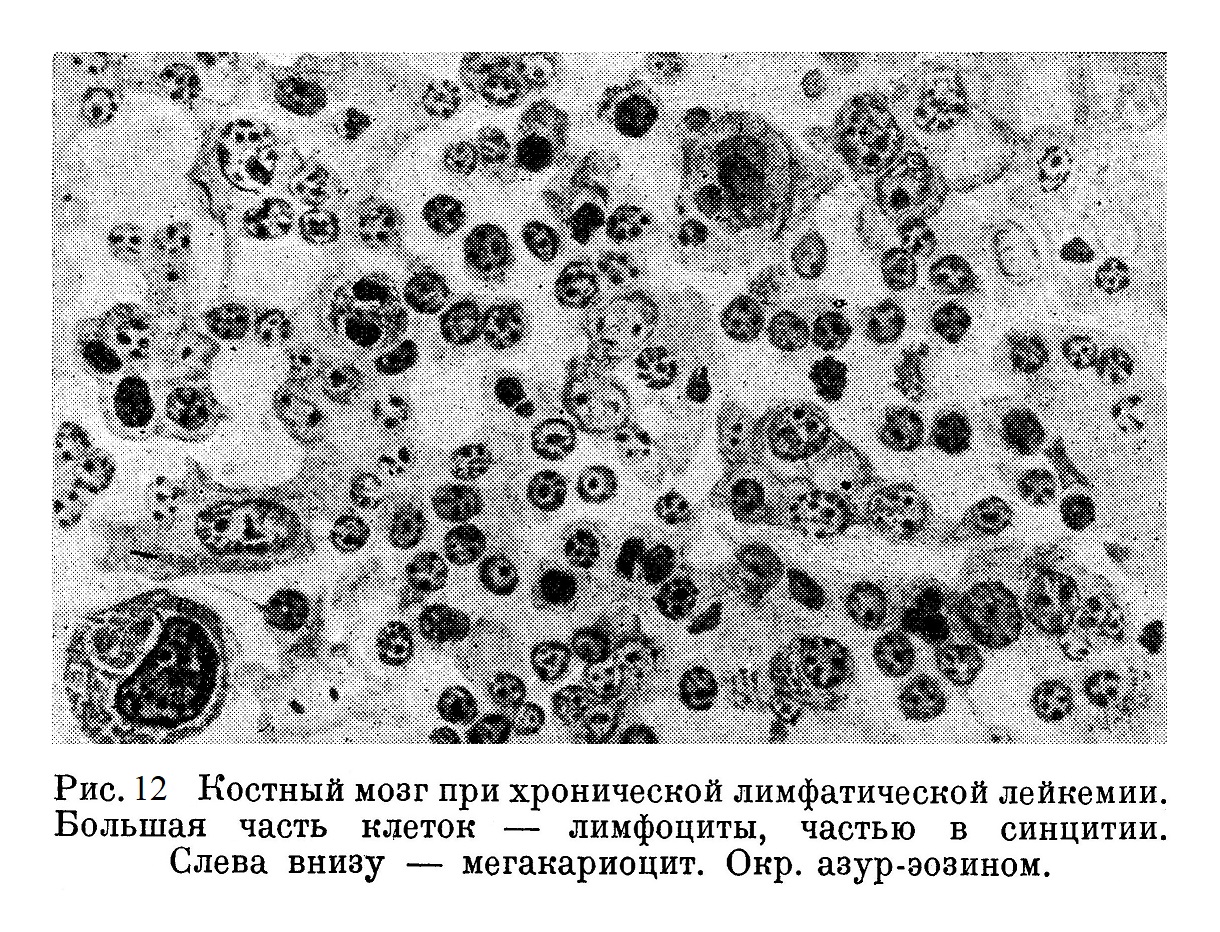
Хотелось бы подчеркнуть одну деталь, демонстративно выступавшую на отдельных участках: клетки-гиганты — мегакариоциты — как бы висят на остове ретикулярной сети, от которой они не успели отделиться (рис. 11). То же самое можно сказать и об отдельных миэлоцитах, имеющих своим основанием reticulum. Местами обнаруживаются небольшие группы миэлобластов, как бы соединенные в небольшом синцитии. На участках, более бедных клетками, выступает сочный протоплазматический reticulum.
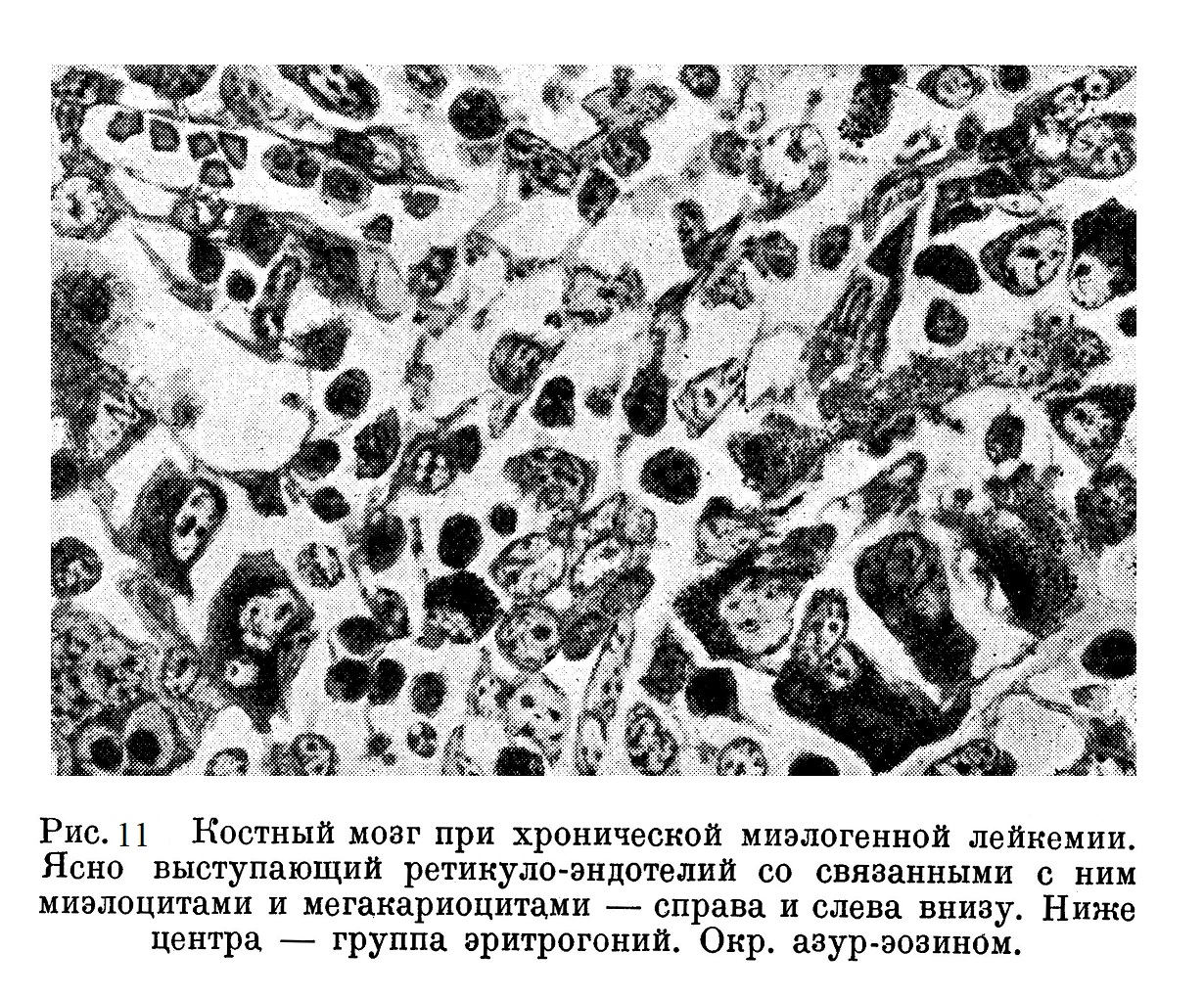
На рис. 12 изображен лимфоидный костный мозг (поздняя стация лимфатической лейкемии); характерно, что почти все лимфоциты зрелые, с однотипно структуированным ядром. И здесь можно обнаружить синцитиальные образования из крупных лимфобластов. Таким образом, при нарушении динамики кроветворения мы во всех системах (эритробластической, лейко- и лимфобластической) обнаруживаем постоянную структурную единицу развития — характерный синцитий, лежащий в основе роста и диференциации ретикуло-эндотелиальной системы.
Pop делит ретикулярные клетки костного мозга на: 1) лимфоидные, 2) плазматические и 3) фагоцитирующие ретикулярные клетки. Мы считаем такую классификацию неправильной потому, что лимфоидные и плазматические клетки являются особо диференцированными элементами и являются, таким образом, уже производными ретикуло-эндотелия.
Норденсон описывает пунктате костного мозга переход ретикулярных клеток в клетки крови.
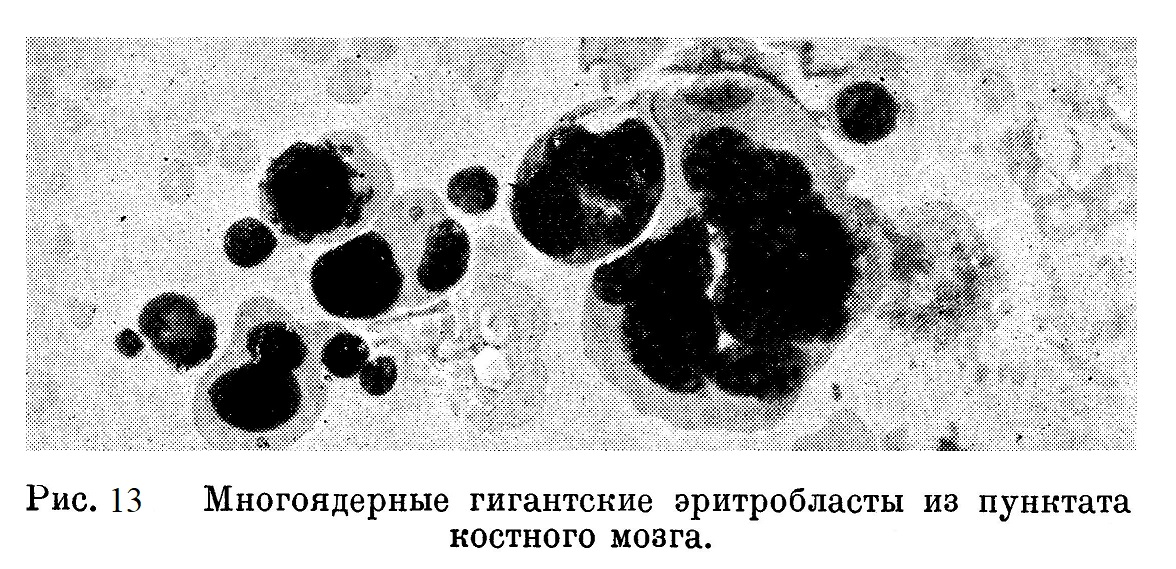
Изучая в порядке консультации с Е. Л. Шварцман пунктат костного мозга при эритробластозе с большим количеством гигантских многоядерных эритробластов (рис. 13), мы могли установить не вызывающие никакого сомнения переходные стадии от ретикуло-эндотелиальных клеток до мегалобластов. Зегердаль и Шлайхер (Segerdahl, Schleicher) наблюдали в проэритробластах пунктата костного мозга «азурофильную зернистость».
Выработка иммунных тел костным мозгом связывается с гранулоцитарной системой. Миэлобласты в смысле ферментативной и иммунобиологической функции являются неактивными, они начинают функционировать только по мере их дальнейшей диференциации. Поэтому клеточный, но миэлобластический костный мозг является неактивным, функционально равноценным апластическому костному мозгу. Миэлогенные элементы реактивно изменяются, только будучи в органической связи с костномозговой тканью; в циркулирующей крови они действуют только теми веществами, которые они выработали в костном мозгу. К таким веществам относится также так называемая токсическая, или патологическая, зернистость. В этом можно убедиться на мазках костного мозга, полученных прижизненно путем пункции или во время операции или же взятых непосредственно после смерти.
Томмсен считает, что токсичная (патологическая) зернистость нейтрофилов не имеется преформированно в лейкоцитах, а образуется в них в момент приготовления мазка.
Мы считаем необоснованным утверждение Рора и некоторых других . авторов, что посмертное исследование костного мозга не соответствует прижизненной его картине, так как быстро наступающий аутолиз уничтожает зернистость лейкоцитов, а все ядра становятся круглыми. Это утверждение основано на исследовании мазков костного мозга. Клетки действительно делаются менее резистентными к механическому воздействию, поэтому иногда из очень большого количества приготовленных мазков только единичные получаются с хорошо сохранившимися клетками. Совсем другая картина получается на срезах. Мы всегда стараемся производить вскрытие со специальным изучением костного мозга через несколько часов после смерти, но все же нередко приходится вскрывать и на следующий день. И все же при хорошей фиксации и хорошей заливке препаратов мы получаем прекрасно сохранившиеся клетки и зернистость. В мазках мы получаем сохранившиеся нейтрофилы даже через двое суток.
Как функциональные пробы для костного мозга предложены впрыскивания 40% раствора желатины [Декастелло (Decastello) и Крюков], нуклеиновой кислоты и 5 % нуклеинового кислого натрия 10 см3 [Габертен (Habertin)]. По данным последнего автора, наивысший лейкоцитоз получается приблизительно через 48 часов — количество лейкоцитов в 2—З раза превышает исходные цифры. При пернициозной анемии, раке, хлорозе, при лейкемии, брюшном тифе и при циррозе печени получается обратная реакция — количество лейкоцитов понижается.
Симпатическое раздражение пилокарпином дает увеличение молодых клеток. Вызывая искусственно ацидоз, Гоф (Hoff) получил у людей лейкоцитоз и увеличение количества кровяных пластинок [Штайнмауер (Steinmauer)].
Усиление функции костного мозга наступает после экстирпации здоровой селезенки (вследствие разрыва от травмы); в крови появляется значительное количество телец Жолли, иногда нормобласты, небольшой лейкоцитоз и тромбоцитоз. Значительно более резкие сдвиги получаются после удаления большой патологически измененной селезенки.
Интересно уяснить себе, как происходит в фолликулах образование лимфоцитов. Мы видели, что на ранних стадиях эмбрионального развития имеется диффузное разрастание лимфоидной ткани и только значительно позже появляются фолликулы. К концу эмбриональной жизни фолликулярный аппарат хорошо развит, но нигде нет центров размножения. Центрами размножения называются скопления больших светлых клеток, находящиеся посредине фолликула (рис. 14). Из этого ясно, что размножение лимфоцитов идет во всяком случае и помимо центров размножения непосредственным делением малых лимфоцитов, которые в свою очередь происходят из недиференцированных клеток ретикулярной основы фолликула. Гельман (Hellmann) считает, что так называемые центры размножения совсем не продуцируют лимфоцитов, а являются выражением реакции аденоидной ткани на токсические вещества; поэтому он предлагает называть их центрами реакции. Несомненно, функция зародышевых центров фолликулов особая. При различных инфекционно- и химически-токсических процессах наблюдается увеличение центров с последующим пикнозом ядер ретикулярных клеток, с кариорексисом (дифтерия, мышьяк, бензол и др.). Большое накопление эритроцитов в синусах лимфатических желез делает их красными, эндотелий сосудов поглощает эритроциты (эритрофагия), гипертрофируется, становится многоядерным. При патологических процессах, особенно связанных с усиленной гибелью эритроцитов, нам приходилось наблюдать превращение эндотелия синусов в объемистые синцитиальные образования с эритро- и лейкофагией.

Абрикосов приводит гигантоклеточную гиперплазию эндотелия синусов лимфатической железы при стрептококковом сепсисе и говорит, что в некоторых случаях в синусах возникает «диференцировка клеток в эритропо-этические и лейкопоэтические формы». При брюшном тифе ретикулярные клетки лимфатических желез гипертрофируются, фагоцитируют лимфоциты и эритроциты — это так называемые «тифозные клетки». Такие же клетки мы наблюдаем при рассасывании пакетов увеличенных лимфатических желез при лейкемии, а также лейкеминеских разрастаний в коже и в костном мозгу.
Из того, что до настоящего времени еще не прекращаются споры по поводу толкования самых основ структуры кроветворных органов, следует, как мало мы осведомлены о деталях процесса кроветворения. Однако основное направление развития ясно: если недиференцированная клетка начала диференцироваться в определенном направлении, никакого возврата к первоначальному состоянию или же перехода к новому типу диференциации быть не может. Поэтому крайне трудно понять, почему Максимов так настойчиво старается доказать, что мезенхимальная клетка сначала диференцируется в лимфоцит, а уже из него получаются другие клетки совершенно другого типа. В последние годы Максимов в культурах тканей пытался воздействием экстракта костного мозга перевести лимфоциты лимфатической железы в миэлоциты и лейкоциты. Он считает, что опыт ему удался: в ткани лимфатической железы наряду с лимфоцитами появились нейтрофильные и эозинофильные миэлоциты, причем автор видит как бы переходные формы между лимфоцитами и миэлоцитами. Но здесь же имелись ретикулярные клетки и, нужно думать, еще менее диференцированные клетки — мезенхимальные; дериватами каких клеток явились эти миэлоциты, сказать, конечно, очень трудно.
Эндотелий первых кровеносных сосудов и первые кровяные тельца (мегалобласты) образуются из мезенхимальных клеток. Затем из мезенхимальных клеток формируется всяретикуло-эндотелиальная система, остающаяся функционирующей на все время постэмбриональной жизни в виде ретикулярных петель, эндотелия венозных капилляров (синусов) кроветворных органов. Таким образом, кроветворение, согласно нашим положениям, происходит следующим образом:
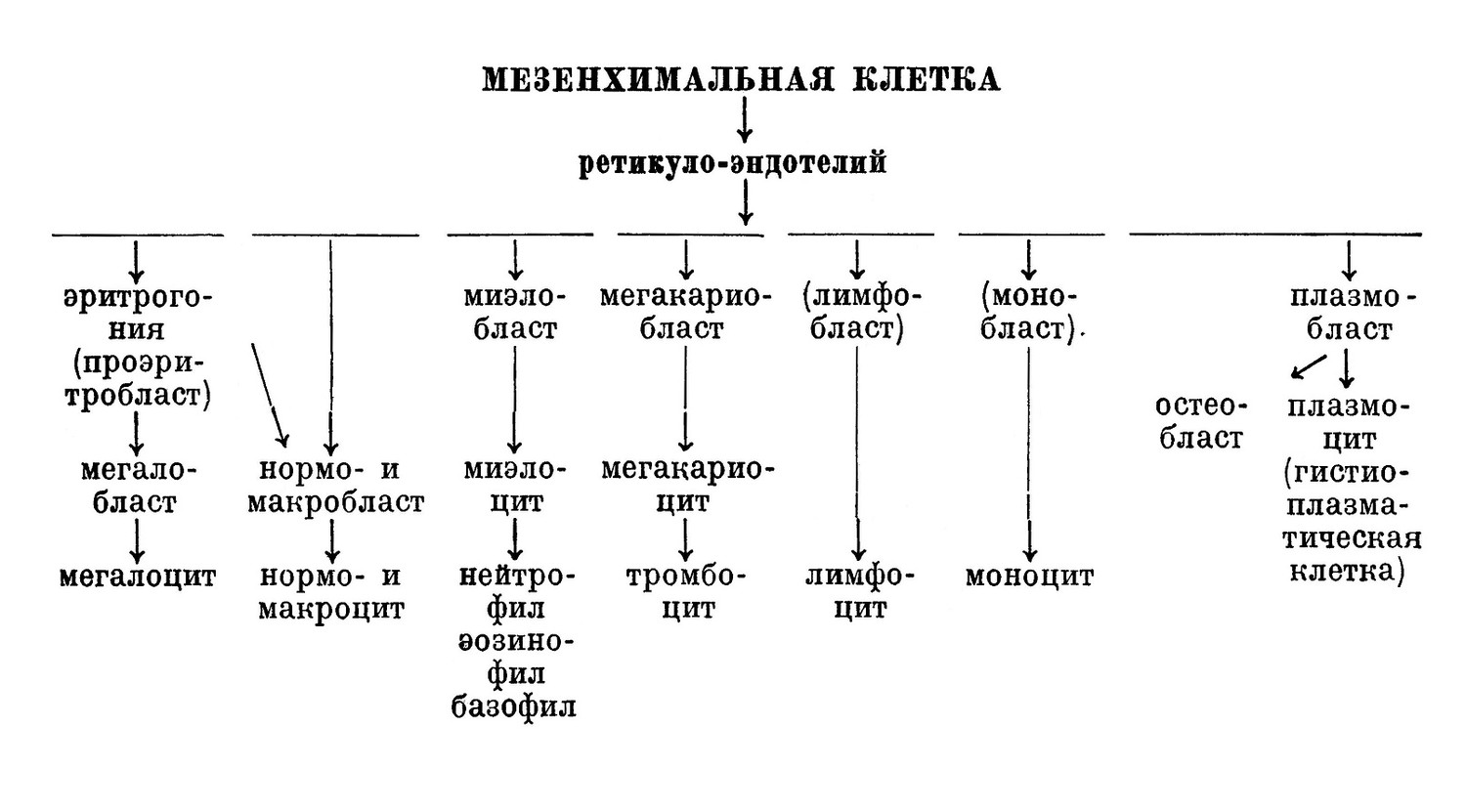
Диференциация мезенхимальных клеток в ретикуло-эндотелий проходит только в зародышевом периоде. Постэмбрионально кроветворная функция полностью осуществляется ретикуло-эндотелиальной системой. Основное разногласие между различными авторами заключается в том, что они признают непосредственный переход мезенхимальных клеток эмбриона в различные виды кровяных клеток, причем постэмбрионально каждый вид клеток развивается уже из детерминированной клетки (эритробласт, миэдобласт, лимфобласт) — полифилетическая теория (Эрлих, Негели, Моравиц и др.). Согласно дуалистической теории Шридде (Schridde), из миэлобласта диференцируются гранулоциты, моноциты и эритробласты, поэтому мезенхимальная клетка, по мнению этих авторов, эмбрионально диференцируется только в миэлобласт и лимфобласт. Триалисты отличаются от дуалистов тем, что они признают, что и эмбрионально, и постэмбрионально моноциты образуются ретикуло-эндотелием. Наконец, согласно монофилетической теории, мезенхимальная клетка сначала диференцируется в гемоцитобласт, клетку, остающуюся в смысле кроветворения омнипотентной в течение всей жизни индивидуума. Максимов, Дауни (Downey) и Вайденрайх считали, что омнипотентным является лимфоцит, циркулирующий в крови. В своей последней монографической работе 1927 г. Максимов признает, что родоначальником первичных эритробластов является гистиобласт, непосредственно диференцировавшийсй из мезенхимальных клеток и не имеющий ничего общего с лимфоцитом. Однако Максимов, точно так же как и Дауни, и Вайденрайх, все же не отказывается от мнения, что на более поздних стадиях развития лимфоцит, циркулирующий в крови, способен диференцироваться в миэлогенные элементы. Кеннингхэм (Cunningham), Сэбин и Доун считают, что в костном мозгу все клетки происходят из одной родоначальной клетки, которая в свою очередь происходит из ретикулярных клеток. Эритробласты, по их мнению, происходят исключительно интраваскулярно из эндотелиальных клеток. Пиней (Ріпеу) производит кровяные клетки непосредственно из ретикуло-эндотелия.
Как уже сказано выше, большинство авторов считает, что регенерация крови постэмбрионально в норме идет только за счет уже имеющихся строго диференцированных клеток. Это положение логически привело Максимова к признанию за лимфоцитами способности производить все миэлоидного рода элементы. И в самом деле, в известном опыте с перевязкой вены почки и инфарцированном участке почки образуется кость с вполне развитым костным мозгом. Из каких же элементов развился костный мозг? Ведь в циркулирующей крови нет ни эритробластов, ни миэлобластов. Максимова этот эксперимент убеждал в том, что из лимфоцита образовались здесь все элементы костного мозга. Тот же самый процесс наблюдается при окостенении тиреоидального хряща с образованием костного мозга. Гистолога эти факты приводят в недоумение; патологоанатому приходится ежедневно наблюдать развитие доиэлогенных очагов в различных органах и тканях — так называемые очаги экстрамедуллярного кроветворения. Печень, селезенка, лимфатические железы становятся органами миэлогенного кроветворения — это называют миэлогенной метаплазией с возвратом к эмбриональному морфологическому строению и функции («морфологический и функциональный атавизм», по выражению Негели). Все эти трудности и, я бы сказала, надуманности отпадают сами собой, если признать кроветворную функцию ретикуло-эндотелия, темпы и качества функциональной деятельности которого регулируются получаемыми им раздражениями. Заварзин также стоит на точке зрения образования всех форменных кровяных элементов эмбрионально из гемоцитобластов: «Не все первичные кровяные клетки расходуются на образование первичных эритробластов. Часть гемоцитобластов остается в недиференцированном состоянии и дает начало накоплениям недиференцированных блуждающих элементов, расселяющихся по всей соединительной ткани и крови. Эти клетки и становятся родоначальными элементами всех дальнейших кроветворных процессов. Поэтому они и получили название гемоцитобластов». Постнатально, по Заварзину, кроветворение идет из эмбрионального запаса эритробластических, лейкобластических и лимфобластических форм. Он не отрицает, однако, образования кровяных клеток и из ретикуло-эндотелия: в нормальных условиях в костном мозгу содержится огромное количество почти готового резервного материала для пополнения убыли в эритроцитах, из которого может весьма быстро восстановиться нормальное число эритроцитов крови даже при значительных кровопотерях. В этих случаях на пополнение убыли эритроцитов в крови растрачивается большая или меньшая масса эритробластов, и тогда начинается восстановление их запаса путем размножения гемоцитобластов и даже их новообразование из ретикулярного, синцития и мезенхимальных элементов. «В нормальном костном мозгу содержатся главным образом метамиэлоциты и готовые молодые лейкоциты. Таким образом, и в этом случае, так же как и в случае эритробластов, в костном мозгу содержится почти вполне готовый резерв, из которого быстро пополняется всякая убыль специальных лейкоцитов».
 Занятие 1-е. Вакцины и анатоксины. Вопросы для обсуждения. 1. Искусственный иммунитет, активный и пассивный. 2. Препараты для создания искусственного активного иммунитета: вакцины и анатоксины. 3. Виды вакцин: живые, убитые и химические. 4. Способы приготовления вакцин. 5. Анатоксины нативные и очищенные, их получение и титрован... Читать далее... |
|